��Ŀ����
��5�֣�̼Ԫ��������������ʵĻ���Ԫ�ء�
��1��д����Ȼ���м�����ȫȼ�յĻ�ѧ����ʽ ��
��2�������±�����ú��ȣ�����Ȼ����ȼ�ϵ��ŵ��� ��
| | 1g������ȫȼ�� | |
| ����������̼������/g | �ų�������/kJ | |
| ���� | 2.75 | 56 |
| ̼ | 3.67 | 32 |
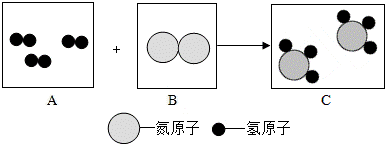
��3��Ϊ���ú�������ʣ��ɽ���ת��Ϊ��ȼ�����壬�÷�Ӧ����ʾ��ͼ���£���������ķ��Ӹ�����Ϊ ��

��4��Һ̬������̼�������˾ȵ����ҷ����Ļ��֣�����˵����ȷ���� ������ĸ��ţ���
A��Һ̬������̼��������Ⱦ����
B��������̼�ɸ����ڿ�ȼ����棬��������
C��Һ̬������̼����ʱ���ȣ����Ϳ�ȼ����Ż��
��5���ڸ��¸�ѹ�£�CO2��NH3���Ժϳ�����[CO(NH2)2]��ͬʱ����ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��1��CH4 + 2O2 CO2 + 2H2O
CO2 + 2H2O
��2������������Ȼ����ú��ȫȼ�գ���Ȼ��ȼ�ղ���������̼����������ú���ų�����������ú����3��1:1 �� ��4��AB �� ��5�� CO2 + 2NH3 CO(NH2)2 + H2O
CO(NH2)2 + H2O
���������������1����Ȼ���м�������������ȫȼ�����ɶ�����̼��ˮ����2���ɱ��е����ݿ�֪������Ȼ����ȼ�ϵ��ŵ��ǵ���������Ȼ����ú��ȫȼ�գ���Ȼ��ȼ�ղ���������̼����������ú���ų�����������ú����3�����������غ㶨�ɣ���ѧ��Ӧǰ��ԭ�Ӹ������䣬�����ɵ�C��D�ķ��Ӹ�����Ϊ1:1����4��Һ̬������̼�������˾ȵ����ҷ����Ļ�������Ϊ��Һ̬������̼������������壬������Ⱦ������������̼��ȼ��Ҳ��֧��ȼ�գ��ܶȱȿ����ɸ����ڿ�ȼ����棬������������ѡAB����5���ڸ��¸�ѹ�£�CO2��NH3���Ժϳ�����[CO(NH2)2]��ͬʱ����ˮ����Ӧ������P��Ӧ������֪����ȷ��д��ѧ����ʽ����.
���㣺��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ������ȼ�ϵ�ʹ������Ի�����Ӱ��.

 ����������ϵ�д�
����������ϵ�д�


 ��ʾһ��Ԫ�ص��������ӣ���������ͬһ��Ԫ�ص������� ��
��ʾһ��Ԫ�ص��������ӣ���������ͬһ��Ԫ�ص������� ��