题目内容
【题目】已知:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑.为了证明过氧化钠(Na2O2)固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣小组的同学利用如图所示实验装置进行探究活动。(铁架台等已略去)
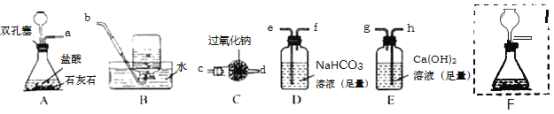
(1)A装置中所发生反应的化学方程式为_____。
(2)请将如图F方框中A装置的长颈漏斗和玻璃导管补画完整_____。
(3)D装置的作用是_____。E装置中可能发生的有关反应的化学方程式为_____。
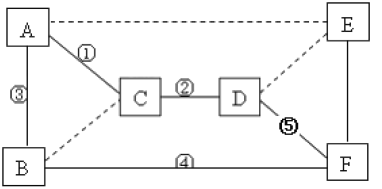
(4)为了达到实验的目的,以上装置导管接口正确的连接顺序为a接_____、_____接_____、_____接_____、_____接b。
(5)氧气可采用B装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?_____
(6)实验结束后,取C装置中固体溶于水,无气泡产生。请设计实验,检验C装置中固体的成分。_____(简要写出实验步骤、现象和结论)。
(7)某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,假如所需要的氧气全部由Na2O2与CO2反应来提供,则该潜水艇一天所需要Na2O2的质量是多少?_____
【答案】CaCO3+2HCl═CaCl2+H2O+CO2↑ 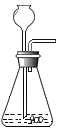 除去HCl气体 Ca(OH)2+CO2=CaCO3↓+H2O e f c d h g 不易溶解于水且支持燃烧 取所得溶液,加入足量的氯化钙溶液,有沉淀生成,取上层清液,滴入酚酞试液,酚酞试液变红,说明C装置中固体的成分为碳酸钠和氢氧化钠 702kg
除去HCl气体 Ca(OH)2+CO2=CaCO3↓+H2O e f c d h g 不易溶解于水且支持燃烧 取所得溶液,加入足量的氯化钙溶液,有沉淀生成,取上层清液,滴入酚酞试液,酚酞试液变红,说明C装置中固体的成分为碳酸钠和氢氧化钠 702kg
【解析】
实验为了证明过氧化钠(Na2O2)固体可在呼吸面具和潜水艇中做供氧剂,是制取二氧化碳然后与过氧化钠反应,证明过程中生成了氧气而消耗了二氧化碳。
(1)A装置中是制取二氧化碳,所以是石灰石和盐酸反应生成氯化钙和水以及二氧化碳,化学方程式为![]() 。
。
(2)由于长颈漏斗需要插入到液面以下,而导气管露出少许即可,所以图F方框中A装置的长颈漏斗和玻璃导管补画完整为:
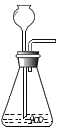
(3)由于生成的气体中混有HCl,所以D装置的作用是 除去HCl气体。E装置中是检验二氧化碳是否还有,也就是证明消耗了二氧化碳而生成了氧气,所以可能发生的有关反应的化学方程式为![]() 。
。
(4)为了达到实验的目的,需要制备二氧化碳且除去杂质后让二氧化碳和过氧化钠反应,进而检验二氧化碳是否有剩余和检验是否生成了氧气,所以以上装置导管接口正确的连接顺序为a接 e、f接 c、d接 h、g接b。
(5)氧气可采用B装置收集说明氧气不易溶解于水,并用带火星的木条检验说明氧气支持燃烧,这是利用了氧气的不易溶解于水且支持燃烧的性质。
(6)实验结束后,取C装置中固体溶于水,无气泡产生。根据给出的信息可能生成了碳酸钠和氢氧化钠,也就是确定固体有碳酸钠和氢氧化钠。不能直接借助碱性进行确定,因为两者均为碱性。应该先检验碳酸钠后检验氢氧化钠,过程中注意不要对氢氧化钠的检验造成干扰。具体实验过程为:取所得溶液,加入足量的氯化钙溶液,有沉淀生成,取上层清液,滴入酚酞试液,酚酞试液变红,说明C装置中固体的成分为碳酸钠和氢氧化钠。
(7)某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,则每天所需要的氧气的质量为100×0.001kg×60×24=144kg
设需要Na2O2的质量为x
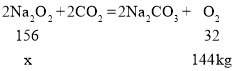
![]()
故潜水艇一天所需要Na2O2的质量是702kg。