��Ŀ����
����Ŀ���ҹ������߳���3.2��ǧ�ף�����ר����������Ա������������Դ�ḻ��������ǰ��ʮ��Զ��
��1���ҹ����������3ǧ����֣��������һλ��Ŀǰ�Ӻ�ˮ����ȡʵ��ķ�����ҪΪ������������������£�  ���������дٽ�ˮ����������Ҫ�����������и����е�����ѡ����ţ�
���������дٽ�ˮ����������Ҫ�����������и����е�����ѡ����ţ�
�ٳ�ϫ�ܢ������ܢ۵��ܢ�̫���ܢݻ�ѧ��
��2������þ�㷺Ӧ�����������������ҵ����±ˮ����ȡþ�Ĺ�����ͼ��ʾ�� ![]()
������ת�������У��ٴ������ķ�Ӧ������Ӧ������к͡����ֽ⡱���ϡ��ֽ⡱��
��3����ˮ�г����̺���������Ԫ�غ�þԪ���⣬�����д����ļ�Ԫ�أ�KC1��KNO3���ܽ��������ͼ��ʾ���Իش��������⣺ ��t1��ʱ��KC1������Һ��������������KNO3������Һ��������������������ڡ���С�ڡ����ڡ�����
����֪20��ʱ��KNO3���ܽ��Ϊ31.6g��80��ʱ��KNO3���ܽ��Ϊ169g����20��ʱ����ʢ��200gˮ���ձ��м���80gKNO3 �� ����ܽ⣬�õ����¶�ʱKNO3��������͡������͡�����Һ��
����KNO3�����л�����������Ϊ���壬������ȥKC1�ķ����� �� 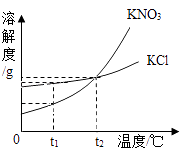
���𰸡�
��1����
��2�����ֽ�
��3�����ڣ����ͣ���ȴ�ȱ�����Һ�����½ᾧ����
���������⣺��1��̫������ȡ֮������֮���ߵ������Դ���������������дٽ�ˮ����������Ҫ��������̫���ܣ���ѡ���ܣ���2���ٴ������ķ�Ӧ���Ȼ�þ���������Ʒ�Ӧ����������þ�������Ȼ��ƣ����ڸ��ֽⷴӦ����3����ͨ�������ܽ�����ߣ����Կ�����t1��ʱ���Ȼ��ص��ܽ�ȴ�������ص��ܽ�ȣ�����KCl������Һ������������������KNO3������Һ���������������� ��20��ʱ��KNO3���ܽ��Ϊ31.6g��80��ʱ��KNO3���ܽ��Ϊ169g����20��ʱ����ʢ��200gˮ���ձ��м���80gKNO3 �� �ܽ�������Ϊ63.2g�����Եõ����¶�ʱKNO3�ı�����Һ��
�����¶������ܽ��������������棬�����������¶�Ӱ��С�����ʣ���������ȴ�ȱ�����Һ���½ᾧ�ķ����ᴿ��
���Դ��ǣ���1���ܣ���2�����ֽ⣻��3���ٴ��ڣ��ڱ��ͣ�����ȴ�ȱ�����Һ�����½ᾧ������
�����㾫����������Ĺؼ���������ᾧ��ԭ������������Ӧ�õ����֪ʶ�����սᾧ�����ַ����������ܼ�����NaCl����ˮɹ�Σ��ͽ����¶ȣ���ȴ�ȵı�����Һ����KNO3�����Լ��Թ����ܽ�����������õ����⣬�˽�1������ָ���¶�ʱ���ʵ��ܽ�ȣ��������ܽ���ж��ܽ��ԣ�2���Ƚ���ͬ�¶�ʱ����һ���¶ȷ�Χ�ڣ���ͬ�����ܽ�ȵĴ�С��3���ȽϺ�ȷ�����ʵ��ܽ�����¶�Ӱ��ij̶ȣ����ݴ�ȷ�����ʽᾧ����������ᴿ�ķ�����4��ȷ����Һ��״̬�������벻���ͣ���

����Ŀ��ijԪ��R�����ԭ������ΪX��ԭ�Ӻ���������ΪY����R2�����ӵĺ����������Ϊ�� ��
A.X��Y
B.X��Y��2
C.X��Y+2
D.Y��2