题目内容
 15、现代城市中有各类喷泉,其原理都是利用了水的压强差,化学中的喷泉原理与其相似,应用了烧瓶内外的压强差.如图所示,烧杯内盛有NaOH溶液,滴管a中有NaOH溶液,实验时,先从滴管a处挤入几滴NaOH溶液,
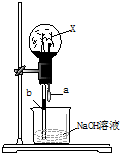
15、现代城市中有各类喷泉,其原理都是利用了水的压强差,化学中的喷泉原理与其相似,应用了烧瓶内外的压强差.如图所示,烧杯内盛有NaOH溶液,滴管a中有NaOH溶液,实验时,先从滴管a处挤入几滴NaOH溶液,随即打开止水夹b,若要形成喷泉,烧瓶内的气体X不可能是( )
分析:本题是利用喷泉实验来考查碱的化学性质,当气体能与碱反应时,造成烧瓶内部压强变小,导致烧瓶内外产生压强差而形成喷泉.
解答:解:A中SO2+2NaOH═Na2SO3+H2O,使烧瓶中气体减少,压强变小,能形成喷泉,故A错误.
B中CO2+2NaOH═Na2CO3+H2O,使烧瓶中气体减少,压强变小,能形成喷泉,故B错误.
C中氢气不与NaOH溶液反应,也不溶解,压强不变,不能形成喷泉,故C正确.
D中HCl+NaOH═NaCl+H2O,使烧瓶中气体减少,压强变小,能形成喷泉,故D错误.
故选C.
B中CO2+2NaOH═Na2CO3+H2O,使烧瓶中气体减少,压强变小,能形成喷泉,故B错误.
C中氢气不与NaOH溶液反应,也不溶解,压强不变,不能形成喷泉,故C正确.
D中HCl+NaOH═NaCl+H2O,使烧瓶中气体减少,压强变小,能形成喷泉,故D错误.
故选C.
点评:本题是根据习题中形成喷泉的信息来考查学生对于碱的化学性质的认识,应紧扣习题信息,来灵活运用化学知识解答.

练习册系列答案
相关题目
 现代城市中有各类喷泉,其原理都是利用了水的压强差,化学中的喷泉原理与其相似,应用了烧瓶内外的压强差.如图所示,烧杯内盛有NaOH溶液,滴管a中有NaOH溶液,实验时,先从滴管a处挤入几滴
现代城市中有各类喷泉,其原理都是利用了水的压强差,化学中的喷泉原理与其相似,应用了烧瓶内外的压强差.如图所示,烧杯内盛有NaOH溶液,滴管a中有NaOH溶液,实验时,先从滴管a处挤入几滴