题目内容
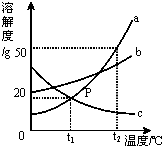 请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题:
(1)P点的含义是______.
(2)t2℃时,30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?______(填“能”或“不能”).
(3)将t2℃时的a、b、c三种物质的饱和溶液降温到t1℃时,溶液中溶质质量分数最小的是______(填写物质序号).
(4)a物质中含有少量的b物质,可采取______的方法(填“降温结晶”、“蒸发结晶”或“过滤”)提纯a物质.
解:(1)a与c的溶解度曲线相交于P点,所以P点表示:t1℃时,a、c的溶解度相等;
(2)t2℃时a的溶解度是50g,所以30g a物质加入到50g水中不断搅拌,最多溶解25g,溶液质量为75g,不能形成80g溶液;
(3)ab的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,饱和时质量分数的计算式 ×100%,可知溶解度大则溶质的质量分数大;所以将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶质质量分数不变,c析出晶体,溶质的质量分数减小,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以三种溶液的溶质质量分数大小关系是b>a>c,最小的是c;
×100%,可知溶解度大则溶质的质量分数大;所以将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶质质量分数不变,c析出晶体,溶质的质量分数减小,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以三种溶液的溶质质量分数大小关系是b>a>c,最小的是c;
(4)a的溶解度受温度影响较大,b的溶解度受温度影响较小,所以a物质中含有少量的b物质,可采取降温结晶的方法;
故答案为:(1)t1℃时,a、c的溶解度相等;
(2)不能;
(3)c;
(4)降温结晶.
分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)据该温度下物质的溶解度分析解答;
(3)据物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答;
(4)据物质的溶解度随温度变化情况分析提纯物质的方法.
点评:了解溶解度的概念、溶解度曲线的意义并会灵活运用知识解决相关问题,考查了学生分析、解答问题的能力.
(2)t2℃时a的溶解度是50g,所以30g a物质加入到50g水中不断搅拌,最多溶解25g,溶液质量为75g,不能形成80g溶液;
(3)ab的溶解度随温度的升高而增大,c的溶解度随温度的升高而减小,饱和时质量分数的计算式
 ×100%,可知溶解度大则溶质的质量分数大;所以将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶质质量分数不变,c析出晶体,溶质的质量分数减小,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以三种溶液的溶质质量分数大小关系是b>a>c,最小的是c;
×100%,可知溶解度大则溶质的质量分数大;所以将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,ab的溶质质量分数不变,c析出晶体,溶质的质量分数减小,t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以三种溶液的溶质质量分数大小关系是b>a>c,最小的是c;(4)a的溶解度受温度影响较大,b的溶解度受温度影响较小,所以a物质中含有少量的b物质,可采取降温结晶的方法;
故答案为:(1)t1℃时,a、c的溶解度相等;
(2)不能;
(3)c;
(4)降温结晶.
分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)据该温度下物质的溶解度分析解答;
(3)据物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答;
(4)据物质的溶解度随温度变化情况分析提纯物质的方法.
点评:了解溶解度的概念、溶解度曲线的意义并会灵活运用知识解决相关问题,考查了学生分析、解答问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题: (2012?平原县一模)请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题:
(2012?平原县一模)请根据右图中a、b、c三种物质的溶解度曲线,回答下列问题:

