题目内容
【题目】CO2是一种宝贵的碳氧资源。某兴趣小组对CO2的研究如下:
已知:常温下,CO2难溶于饱和NaHCO3溶液。
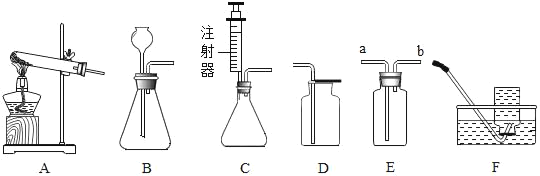
Ⅰ.CO2的制备和收集:
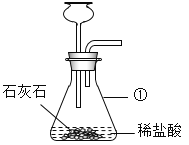
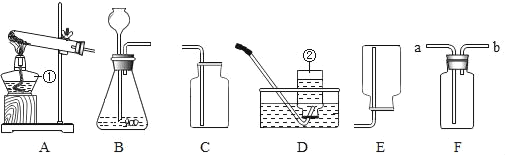
(1)写出图中标号仪器的名称:①_____。
(2)写出用石灰石和稀盐酸制取CO2的化学方程式_____。图中装置有一处明显的错误是_____。
(3)常温下,下列收集CO2的方法中可行的是_____(填字母)。
a.向上排空气法 b.向下排空气法 c.排饱和NaHCO3溶液法
Ⅱ.CO2的利用:
全球能源生产正向“氢能经济”转型,以CO2和可再生生物资源(如纤维素等)为原料生产氢气已成为能源研究的重点。下图是某新型能源转换与利用模式示意图:

(4)该模式中涉及的能源转化依次为:太阳能→生物质能→氢能→_____。
(5)该系统中循环使用的物质是_____。
(6)与电解水相比,该模式制取氢气的主要优点是_____。
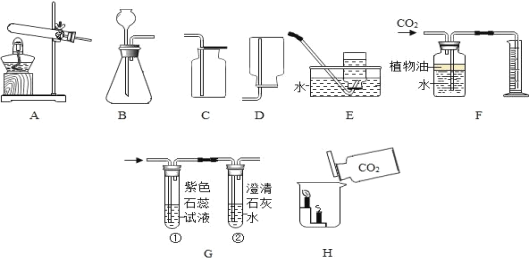
Ⅲ.探究CO2与NaOH的反应:
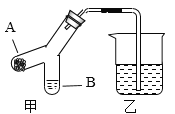
(7)如图装置,气密性良好。在A处放置适量干冰,B处装入适量的浓NaOH溶液,烧杯中加入足量的稀盐酸。实验过程中,观察到乙中导管口有气泡冒出,原因是_____。
(8)一段时间后,观察到的现象是:乙中_____,B中_____,说明CO2与NaOH发生反应,写出CO2与NaOH反应方程式为_____。
【答案】锥形瓶 CaCO3+2HCl=CaCl2+H2O+CO2↑ 长颈漏斗下端未液封 ac 电能 CO2 节约能源 干冰升华(产生大量气体) 溶液倒吸入B(或甲)中 产生气泡 2NaOH+CO2=Na2CO3+H2O
【解析】
(1)根据图示,该仪器名称为锥形瓶;
(2)石灰石和稀盐酸反应生成氯化钙、水和二氧化碳,故填![]() ;长颈漏斗下端未深入到液面下液封,产生的二氧化碳会从长颈漏斗处流出;
;长颈漏斗下端未深入到液面下液封,产生的二氧化碳会从长颈漏斗处流出;
(3)因为二氧化碳密度高于空气,并且不与饱和碳酸氢钠溶液反应,故可用向上排空气法和排饱和碳酸氢钠溶液法收集二氧化碳,故选ac;
(4)根据图示,最后转化为电能;
(5)根据图示,该反应中循环的物质为二氧化碳;
(6)该反应较电解水反应,节约电能,利用无污染可再生的太阳能;
(7)A中干冰升华,产生大量二氧化碳气体,使烧杯中有气泡产生;
(8)经过干冰升华后,部分二氧化碳与氢氧化钠溶液反应,生成碳酸钠和水,使甲装置中气压降低,烧杯中溶液倒吸入甲中;当盐酸溶液倒流入B中时,与溶液中碳酸钠反应产生二氧化碳,故B中会产生气泡;氢氧化钠和二氧化碳反应生成碳酸钠和水,故填![]() 。
。