题目内容
【题目】实验室常用下图所示装置测定空气中氧气的含量。

(1)若有1.24 g红磷发生反应,根据化学方程式计算,产生的P2O5有_______g。
(2)该实验中红磷过量,你认为是否有道理?_______(填“是”或“否”),你的理由:___________________________。
(3)在动手实验的过程中,你认为该实验的不足是___________(至少一条)。
【答案】 2.84 是 该实验要测定的是空气中氧气的含量,必须要将集气瓶中的氧气消耗完,所以红磷应过量 红磷被点燃后再伸入集气瓶内,致使部分空气因热膨胀而逸出集气瓶(或磷在空气中燃烧会污染空气;或导气管内存有空气也会影响实验的准确性;或实验误差较大等合理答案均可)
【解析】分析:用红磷燃烧测定空气的组成时,红磷一定要过量,目的是把氧气全部消耗掉;点燃红磷前,弹簧夹要夹紧胶皮管,红磷熄灭后要等集气瓶冷却后再打开弹簧夹等.若预先使导管内充满水,误差会更小.
解答:解:(1)解:设产生固体的质量为X
4P+5O2![]() 2P2O5
2P2O5
124 284
1.24g X
![]() =
=![]()
解得:X═2.84g
答:产生固体的质量为2.84g.
(2)该实验的原理是消耗氧气,使装置内外产生压强差,为了使氧气全部耗尽,因此红磷要过量.
故答案为:是; 红磷过量,尽可能将集气瓶中的氧气消耗完.
(3)该实验注意点很多,排除药品量和装置气密性的影响外,还可从环保、操作等方面考虑.从操作角度看不足为:红磷被点燃后缓慢伸入集气瓶内,致使部分空气因热膨胀而溢出集气瓶;从环保角度考虑不足为:磷在空气中燃烧会污染空气;从利用的装置看导气管内存有空气会使实验误差较大.
故答案为:红磷被点燃后缓慢伸入集气瓶内,致使部分空气因热膨胀而溢出集气瓶(或磷在空气中燃烧会污染空气或导气管内存有空气会使实验误差较大).

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体。
(1)请写出镁条燃烧的符号表达式______________________________;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量。有人认为这个反应不遵循质量守恒定律。你认为出现这样实验结果的原因可能是:_____________________;
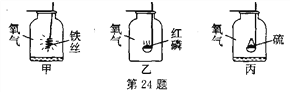
(3)要使该反应能用于验证质量守恒定律,最合理的实验装置是____________(填序号);

(4)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体。

【提出问题】黄色固体是什么?
【查阅资料】(Ⅰ)镁能与二氧化碳反应生成碳和氧化镁;
(Ⅱ)镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;
(Ⅲ)氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
【做出猜想】
猜想一:固体是碳;
猜想二:固体是氧化镁
猜想三:黄色固体是Mg3N2
【实验探究】固体不可能是碳和氧化镁,原因①______________________;
请设计实验,验证猜想:
实验操作 | 实验现象 | 结论 | |
取少量固体于试管中,加水;将湿润的红色石蕊试纸放在试管口 | ②________________ | 该固体是Mg3N2 | |
【反思与交流】空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:③__________________________________。