题目内容
【题目】如图是A、B、C三种物质的溶解度随温度变化的曲线图.根据图回答:
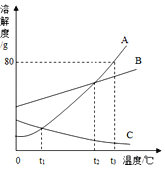
(1)S表示物质的溶解度,当温度为 ℃时SA=SB;
(2)随着温度升高,A、B、C三种物质的饱和溶液中能析出溶质的是 。
(3)B中混有少量的A,欲提纯B,应采用的方法是 (填“降温结晶”或“蒸发结晶”)。
(4)t3℃时,90gA物质的饱和溶液中,含有A物质 g
【答案】(1)t2 (2)C (3)蒸发结晶(4)40
【解析】
试题分析:(1)由图,t2℃时,AB有交点即此温度时溶解度相同;(2)AB随温度升高溶解度升高,无晶体析出,C随温度升高溶解度下降有晶体析出;(3)A的溶解度随温度变化大,B变化小,要提纯B适宜蒸发结晶;(4)t3℃时,A的溶解度为80g;即100g水溶解80gA形成180g的饱和溶液,那么由溶液的均一性90g饱和溶液中溶质应为40g。

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如下图所示的pH曲线,请回答:
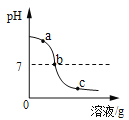
(1)由图可知该实验操作是将__________滴加到另一种溶液中;
(2)该反应的化学方程式为___________;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现___________的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 | 实验现象 | 实验结论 |
另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 | ________ | 该样品为b处溶液。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑____________。