题目内容
(1)天然水受到污染后,净化时需要运用科学的方法,同时要爱护水资源.
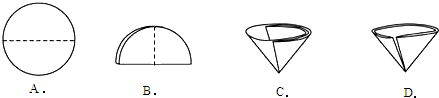
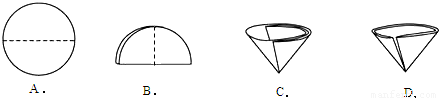
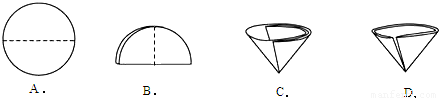
①自来水生产过程中先用________的方法除去水中不溶性杂质,再进行消毒.在操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是________.(填序号).
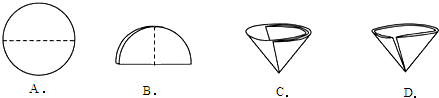
②若发现滤纸和漏斗间有气泡,可能的影响是________,处理的方法是________.
③地下水硬度过大会影响生产和生活,应软化后使用.检验硬水常用的物质是________.
④我市不少村镇小型河沟中藻类疯长,说明水体富营养化,你认为造成该现象的原因可能有________(正确选项有多个,请选填字母序号).
A.化学肥料流失到河中 B.排放的生活污水中有含磷洗涤剂
C.人畜的粪便流失到河中 D.工业废水的排放
⑤爱护水资源从我做起,下列做法可行的有________(正确选项有多个,请选填字母序号).
A.洗脸、刷牙时随时关闭水龙头 B.用洗菜、洗衣的水冲厕所、拖地
C.用洗衣机洗一两件衬衫 D.用残茶水浇灌某些花卉
(2)质量守恒定律的定量研究对化学科学发展具有重大意义.
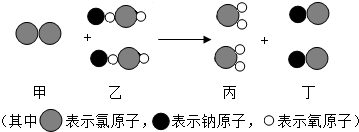
①我国从今年5月1日起,酒驾入刑.“酒精检测仪”可检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4═2Cr2(SO4)3+2CO2↑+9X,反应中红色的CrO3转变为绿色的Cr2(SO4)3,其中X的化学式为________;Cr2(SO4)3中Cr元素的化合价________.
②已知m1g镁条放在空气中完全燃烧,生成m2g氧化镁(不考虑其它反应),m1________m2其化学方程式为________,.小西在做该实验时,用________夹持镁条,点燃,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1>m2,其原因是________.
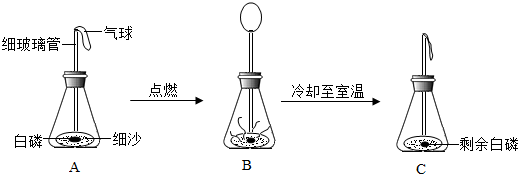
③在用白磷探究质量守恒定律的实验中,晓华同学将橡皮塞上的细玻璃管下端放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示.请回答下列问题:
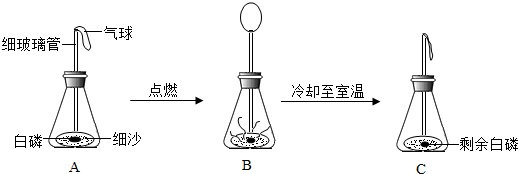
a.实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是________;
b.将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物分析天平平衡的原因是________.
解:(1)①自来水生产过程中先用过滤的方法除去水中不溶性杂质,再进行消毒,在操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是D;
②若发现滤纸和漏斗间有气泡,可能的影响是过滤的速率减慢,处理的方法是用玻璃棒轻压;
③检验硬水常用的物质是肥皂水;
④下列做法:化学肥料流失到河中、排放的生活污水中有含磷洗涤剂、人畜的粪便流失到河中、工业废水的排放都会造成水体富营养化;
⑤下列做法:洗脸、刷牙时随时关闭水龙头,用洗菜、洗衣的水冲厕所、拖地,用残茶水浇灌某些花卉都能节约用水,方法可行;
(2)①根据质量守恒定律可知,X的化学式为:H2O;根据化合价原则可知,Cr2(SO4)3中Cr元素的化合价是+3价;
②根据质量守恒定律可知,m1<m2,其化学方程式为 2Mg+O2 2MgO,小西在做该实验时,用坩埚钳夹持镁条,称量无误时,发现m1>m2,其原因是:生成的氧化镁部分以白烟扩散到空气中;
2MgO,小西在做该实验时,用坩埚钳夹持镁条,称量无误时,发现m1>m2,其原因是:生成的氧化镁部分以白烟扩散到空气中;
③a实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是白磷燃烧消耗氧气,气压减小;
b将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物分析天平平衡的原因是:参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.
故答为:(1)①过滤,D;②速率减慢,用玻璃棒轻压;③肥皂水; ④ABCD; ⑤ABD;
(2)①H2O,+3 ②<,2Mg+O2 2MgO,坩埚钳,生成的氧化镁部分以白烟扩散到空气中;③白磷燃烧消耗氧气,气压减小;参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.
2MgO,坩埚钳,生成的氧化镁部分以白烟扩散到空气中;③白磷燃烧消耗氧气,气压减小;参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.
分析:(1)①根据过滤的原理和过滤器的制作的方法进行分析;②根据过滤器的制作的方法和注意事项进行分析;
③根据硬水和软水的成分进行分析;④根据排放物的成分进行分析;⑤根据做法是否符合节约用水进行分析;
(2)①根据质量守恒定律进行分析,根据化学式和化合价原则判断元素的化合价;②根据质量守恒定律进行分析质量的变化、书写反应的方程式;③a、根据磷与氧气的反应进行分析;b、根据质量守恒定律进行分析.
点评:本题涉及的知识点比较多,都是课本的基础知识,应加强基础知识的学习.
②若发现滤纸和漏斗间有气泡,可能的影响是过滤的速率减慢,处理的方法是用玻璃棒轻压;
③检验硬水常用的物质是肥皂水;
④下列做法:化学肥料流失到河中、排放的生活污水中有含磷洗涤剂、人畜的粪便流失到河中、工业废水的排放都会造成水体富营养化;
⑤下列做法:洗脸、刷牙时随时关闭水龙头,用洗菜、洗衣的水冲厕所、拖地,用残茶水浇灌某些花卉都能节约用水,方法可行;
(2)①根据质量守恒定律可知,X的化学式为:H2O;根据化合价原则可知,Cr2(SO4)3中Cr元素的化合价是+3价;
②根据质量守恒定律可知,m1<m2,其化学方程式为 2Mg+O2
 2MgO,小西在做该实验时,用坩埚钳夹持镁条,称量无误时,发现m1>m2,其原因是:生成的氧化镁部分以白烟扩散到空气中;
2MgO,小西在做该实验时,用坩埚钳夹持镁条,称量无误时,发现m1>m2,其原因是:生成的氧化镁部分以白烟扩散到空气中;③a实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因是白磷燃烧消耗氧气,气压减小;
b将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从具体的反应物和生成物分析天平平衡的原因是:参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.
故答为:(1)①过滤,D;②速率减慢,用玻璃棒轻压;③肥皂水; ④ABCD; ⑤ABD;
(2)①H2O,+3 ②<,2Mg+O2
 2MgO,坩埚钳,生成的氧化镁部分以白烟扩散到空气中;③白磷燃烧消耗氧气,气压减小;参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.
2MgO,坩埚钳,生成的氧化镁部分以白烟扩散到空气中;③白磷燃烧消耗氧气,气压减小;参加反应的白磷和氧气的总质量和生成的五氧化磷的质量相等.分析:(1)①根据过滤的原理和过滤器的制作的方法进行分析;②根据过滤器的制作的方法和注意事项进行分析;
③根据硬水和软水的成分进行分析;④根据排放物的成分进行分析;⑤根据做法是否符合节约用水进行分析;
(2)①根据质量守恒定律进行分析,根据化学式和化合价原则判断元素的化合价;②根据质量守恒定律进行分析质量的变化、书写反应的方程式;③a、根据磷与氧气的反应进行分析;b、根据质量守恒定律进行分析.
点评:本题涉及的知识点比较多,都是课本的基础知识,应加强基础知识的学习.

练习册系列答案
相关题目