题目内容
【题目】(1)现有H、C、O、N四种常见的元素,请选用其中的元素写出符合初中已学物质各一种(用化学式表示):
①电解水正极产生的气体 ;②溶于水后使水温降低的物质 ;
③相对分子质量最小的氧化物 ;④雪碧等汽水中含有的一种酸 。
(2)请写出下列反应的化学方程式。
①加热碱式碳酸铜 ;
②铁丝在纯氧中燃烧 ;
③盐酸除铁锈 ,溶液由无色变为 色。
④将少量二氧化碳通入足量石灰水中 该反应后溶液的质量较反应前 (选填“增加”、“减少” 或“不变”)了。
⑤将少量硫酸铵晶体与熟石灰混合研磨: ;该反应 (填“属于”或“不属于”)复分解反应,生成的气体可用_____________________检验。
【答案】(1)O2; NH4NO3; H2O;H2CO3; (2)Cu2(OH)2CO3![]() 2CuO + H2O + CO2↑;3Fe + 2O2
2CuO + H2O + CO2↑;3Fe + 2O2![]() Fe3O4 Fe2O3+6HCl==2FeCl3+3H2O ;黄色;CO2 +Ca(OH)2 ==CaCO3↓+ H20; 减小;(NH4)2SO4+ Ca(OH)2= CaSO4+2NH3↑+2H2O;属于;湿润的红色石蕊试纸。
Fe3O4 Fe2O3+6HCl==2FeCl3+3H2O ;黄色;CO2 +Ca(OH)2 ==CaCO3↓+ H20; 减小;(NH4)2SO4+ Ca(OH)2= CaSO4+2NH3↑+2H2O;属于;湿润的红色石蕊试纸。
【解析】
试题分析:(1) ①电解水正极产生的气体O2;②溶于水后使水温降低的物质NH4NO3;③相对分子质量最小的氧化物 H2O;④雪碧等汽水中含有的一种酸H2CO3;(2)①加热碱式碳酸铜化学方程式为Cu2(OH)2CO3 △ 2CuO + H2O + CO2↑,②铁丝在纯氧中燃烧的化学方程式为3Fe + 2O2燃点 Fe3O4; ③盐酸除铁锈的化学方程式为Fe2O3+6HCl==2FeCl3+3H2O,因为溶液中含有三价铁离子,故溶液由无色变为黄色;④将少量二氧化碳通入足量石灰水中反映的化学方程式为CO2 +Ca(OH)2 ==CaCO3↓+ H20,该反应后溶液的质量较反应前减小;⑤将少量硫酸铵晶体与熟石灰混合研磨的化学方程式为(NH4)2SO4+ Ca(OH)2= CaSO4+2NH3↑+2H2O,该反应属于复分解反应,生成的气体可用湿润的红色石蕊试纸。

 快乐5加2金卷系列答案
快乐5加2金卷系列答案【题目】用下列物质的序号填空:a.武德合金 b.干冰 c.氢气 d.维生素 e.双氧水
(1)可用作清洁能源的是 ;
(2)可用于人工降雨的是 ;
(3)可用作保险丝的是 ;
(4)可用于实验室制氧气的是 .
【题目】叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。
【查阅资料】:
①NaN3受撞击会迅速分解生成Na、N2,写出该反应的化学方程式 。
②NaN3遇盐酸、H2SO4溶液无气体生成;
③碱石灰是CaO和 NaOH的混合物;
④NaN3工业上制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O = NaN3+NaOH+X;则X的化学式为 。
【问题探究】:(一)测定某工业级NaN3样品中Na2CO3的质量分数
(1)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示) ;
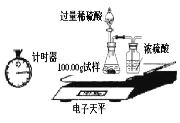
(2)某同学设计如图装置测出碳酸钠的质量分数,其实验数据记录如下:
称量项目 | 称量时间 | 质量(g) |
试样 | 100.00 | |
装置+稀硫酸质量 | 241.20 | |
装置+稀硫酸质量+试样 | 反应开始后15秒 | 339.20 |
装置+稀硫酸质量+试样 | 反应开始后35秒 | 339.00 |
装置+稀硫酸质量+试样 | 反应开始后55秒 | 339.00 |
①写出锥形瓶中发生的反应方程式: ;
②若无浓硫酸的洗气装置,会使测定的结果 (填“偏大”、“偏小”或“不变”);
③利用表中数据计算出碳酸钠的质量分数为 。
【问题探究】:(二)测定某工业级样品中NaN3的质量分数
小谈同学精确称量0.140 g NaN3样品,设计如图装置测定其质量分数。
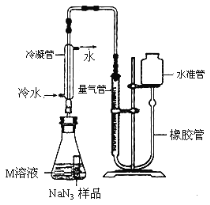
已知2NaN3 → 3N2(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(1)检查该装置气密性的方法是:连接好装置,从水准管注水, ,说明气密性良好。
(2)使用冷水冷凝的目的是: 。
(3)倾斜锥形瓶使小试管中的NaN3样品与M溶液接触充分反应。 常温下测得量气管读数为67.2 mL(N2的密度为1.25 g/L),则实验中选用的量气管规格合适的是_____(填字母序号)。
A.100 mL B.1 L C.2 L
(4)计算工业级样品中NaN3的质量分数(写出计算过程,结果保留0.1%)。