题目内容
为了测定石灰石中碳酸钙的质量分数,某兴趣小组的同学称取石灰石样品12.5g,高温煅烧至质量不再改变,称得剩余固体质量为8.1g(假设杂质不参加反应;发生反应的化学方程式为CaCO3
CaO+CO2↑ ),试计算:
(1)生成二氧化碳质量是 g;
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程)
| ||
(1)生成二氧化碳质量是
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:碳酸钙受热分解生成氧化钙和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量;
根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算石灰石样品中碳酸钙的质量分数.
根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算石灰石样品中碳酸钙的质量分数.
解答:解:(1)生成二氧化碳质量为:12.5g-8.1g=4.4g,
故填:4.4.
(2)设碳酸钙的质量为x,
CaCO3
CaO+CO2↑,
100 44
x 4.4g
=
,
x=10g,
石灰石样品中碳酸钙的质量分数为:
×100%=80%,
答:石灰石样品中碳酸钙的质量分数为80%.
故填:4.4.
(2)设碳酸钙的质量为x,
CaCO3
| ||
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g,
石灰石样品中碳酸钙的质量分数为:
| 10g |
| 12.5g |
答:石灰石样品中碳酸钙的质量分数为80%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
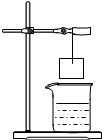 小华将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色.再将其悬挂于铁架台上,并在滤纸的下方放置一盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )
小华将一张滤纸在某指示剂中浸泡后晾干,用蘸有氢氧化钠溶液的玻璃棒在上面写“化学”两字,立刻显红色.再将其悬挂于铁架台上,并在滤纸的下方放置一盛有某溶液的烧杯,过一会儿,发现红色的字消失,则滤纸上的指示剂和烧杯中的溶液分别是( )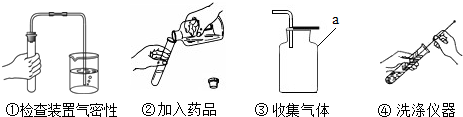
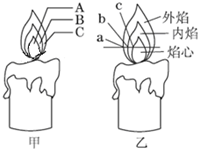 某化学兴趣小组的同学对蜡烛(主要成分为石蜡)及其燃烧进行了如下探究.
某化学兴趣小组的同学对蜡烛(主要成分为石蜡)及其燃烧进行了如下探究.