题目内容
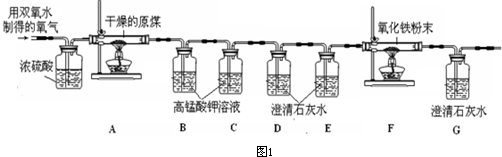
原煤在氧气中不完全燃烧会生成CO、CO2、水蒸汽等混合气体.同学们在实验室欲用下图所示的装置检验生成的CO和CO2气体,准备了如下图所示的装置(其他仪器用品略).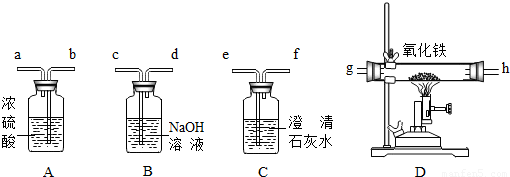
(1)装置A的作用是 .
(2)装置C中发生反应的化学方程式为 .
(3)上述装置组合后还有明显不足之处,你认为不足之处是 .
(4)为达到实验目的,将上述装置组合后进行实验,其接口顺序为:混合气体→ . (填“a~h”接口序号,装置可重复使用,需要有检查气体是否除尽的装置)
【答案】分析:(1)从浓硫酸的吸收性考虑;
(2)二氧化碳与C中的澄清石灰水反应;
(3)从一氧化碳有毒考虑;
(4)根据各自的作用连接,A用于吸收水分,B用于吸收二氧化碳,C用于二氧化碳的检验,D用于一氧化碳的检验.
解答:解:(1)A中的浓硫酸可以吸收水分;故答案为:除水蒸气;
(2)C中的石灰水能用于检验二氧化碳的存在,化学反应式是:Ca(OH)2+CO2═CaCO3↓+H2O;故答案为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)因CO有毒,排放后会污染空气,但装置中没有处理;故答案为:没有进行尾气处理;
(4)将混合气体先ef检验二氧化碳的存在,再通过cd使二氧化碳被NaOH溶液完全吸收,再次通过ef看是否还有二氧化碳,再通过ba吸收可能存在的水分,再将剩余的CO通过gh,最后用再次用ef检验是否二氧化碳生成.故答案为:ef→cd→ef→ba→gh→ef.
点评:本题主要考查气体的除杂和检验,要我们对常见气体的性质特点了然于心方可作对此题.
(2)二氧化碳与C中的澄清石灰水反应;
(3)从一氧化碳有毒考虑;
(4)根据各自的作用连接,A用于吸收水分,B用于吸收二氧化碳,C用于二氧化碳的检验,D用于一氧化碳的检验.
解答:解:(1)A中的浓硫酸可以吸收水分;故答案为:除水蒸气;
(2)C中的石灰水能用于检验二氧化碳的存在,化学反应式是:Ca(OH)2+CO2═CaCO3↓+H2O;故答案为:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)因CO有毒,排放后会污染空气,但装置中没有处理;故答案为:没有进行尾气处理;
(4)将混合气体先ef检验二氧化碳的存在,再通过cd使二氧化碳被NaOH溶液完全吸收,再次通过ef看是否还有二氧化碳,再通过ba吸收可能存在的水分,再将剩余的CO通过gh,最后用再次用ef检验是否二氧化碳生成.故答案为:ef→cd→ef→ba→gh→ef.
点评:本题主要考查气体的除杂和检验,要我们对常见气体的性质特点了然于心方可作对此题.

练习册系列答案
相关题目