��Ŀ����
����Ŀ����ľ̿��ԭ����ͭ��ʵ����ͼ��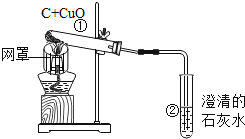
��1���ƾ��Ƽ����ֵ�Ŀ����
��2���տ�ʼԤ�ȣ��Թܢ��������������ݣ���ʯ��ˮ������ǣ�ԭ������
��3���������ȣ��۲쵽ʯ��ˮ����ǣ���ɫ��ĩ�г��ֺ�ɫ���ʣ�����д��������Ӧ�ķ���ʽ������
��4��ֹͣ����ʱ�����Թܢ���ȴ���ٰ��Թ���ķ�ĩ����������������ԭ���� ��
��5���¿κ�ͬѧ����ϸ�۲��Թ��ﵹ���ķ�ĩ�����ֺ�ɫ�ķ�ĩ�л���һЩ��ɫ�ķ�ĩ���ӣ��м�λͬѧ�Ʋ��ɫ��ĩ�ٿ�����û�з�Ӧ���ľ̿��ĩ���ڿ�����û�з�Ӧ�������ͭ��ĩ���ۿ�����û�з�Ӧ���ľ̿������ͭ�Ļ����������ʵ��֤���Ʋ�ٳ�������д�������ʵ�鲽�衢�����ۣ�
���𰸡�
��1�����л��棬�ṩ����
��2���տ�ʼ�Թ��ڵĿ����������ͣ��ų������ǿ���
��3��C+2CuO ![]() 2Cu+CO2����CO2+Ca��OH��2�TCaCO3��+H2O
2Cu+CO2����CO2+Ca��OH��2�TCaCO3��+H2O
��4����ֹ���ɵ�ͭ�ֱ�����������ͭ
��5��ȡ�ú�ɫ��ĩ���ڿ��������գ��۲쵽��ɫ��ĩ����ʧ���Ʋ�ٳ���
��������
��1��ľ̿��ԭ����ͭ�������Ǹ��£��ƾ��ƻ�������һ�����֣�����Ϊ��ʹ���ӻ��漯�У�ʹ�ƾ�ȼ�ճ�֣�����¶ȣ�ʹ����������������£�
��2���տ�ʼ���ȣ��Թ���Ŀ������������ݳ����������ɵĶ�����̼����˳����ʯ��ˮ�в������ݣ��������ʯ��ˮ������ǣ�
��3��ľ̿��һ����ͭ�ڸ�������������ͭ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��C+2CuO ![]() 2Cu+CO2����ʯ��ˮ�е��������������ƣ�����������Ӧ���ɵĶ�����̼��Ӧ����̼��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��
2Cu+CO2����ʯ��ˮ�е��������������ƣ�����������Ӧ���ɵĶ�����̼��Ӧ����̼��ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��CO2+Ca��OH��2�TCaCO3��+H2O��
��4�������ڼ��ȵ������£�ͭ��������е�������Ӧ�����ԣ�ֹͣ����ʱ�����Թܢ���ȴ���ٰ��Թ���ķ�ĩ����������������ԭ���ǣ���ֹ���ɵ�ͭ�ֱ�����������ͭ��
��5������ľ̿ȼ�������˶�����̼�����ԣ����ʵ��Ϊ��ȡ�ú�ɫ��ĩ���ڿ��������գ��۲쵽��ɫ��ĩ����ʧ�����Ʋ�ٳ�����
�����㾫����������Ŀ����֪����������̼�Ļ�ѧ���ʵ����֪ʶ���Եõ�����Ĵ𰸣���Ҫ���ո��ֵ���̼�Ļ�ѧ����ȴ��ȫ��ͬ��1�������µ��ȶ���ǿ2����ȼ��:��ȫȼ��(��������),����CO2������ȫȼ�� (����������),����CO��3����ԭ�ԣ�Ӧ�ã�ұ��ҵ������ɫ��ĩ��ɹ�����ɫ��ʯ��ˮ����ǣ�

