题目内容
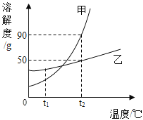
【题目】甲、乙、丙三种固体物质的溶解度曲线如下图所示,请根据图示同答下列问题。
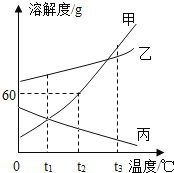
(1)丙物质的溶解度随温度的升高而_____。(填“增大”或“减小”)。
(2)t1℃时,将甲物质的饱和溶液升温到t3℃,所得溶液中溶质的质量分数_____。(填“变大”、“变小”或“不变”)。
(3)t2℃时,将100g水加入到盛有30g甲物质的烧杯中,充分溶解后得到不饱和溶液,若想使溶液恰好饱和,可采用的方法是:_____。
(4)t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是_____。
【答案】减小 不变 加入甲物质30g或蒸发50g水或降低温度 甲>乙>丙
【解析】
(1)从溶解度曲线可以看出:甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度的升高而减小,故填:减小;
(2)甲的溶解度随温度的升高而增大,t1℃时,将甲物质的饱和溶液升温到t3℃,甲的饱和溶液变成甲的不饱和溶液,溶液中溶质的质量分数不变,故填:不变;
(3)从图可以看出:t2℃时,甲的溶解度为60g,即该温度下,100g水中溶解60g甲达到饱和溶液,所以要使溶液恰好饱和,可以加入30g甲。也通过蒸发水达到饱和,饱和溶液中溶质的质量分数为![]() ,设蒸发掉水的质量为x,则
,设蒸发掉水的质量为x,则![]() ,x=50g,即蒸发掉50g水也可以使溶液达到饱和。
,x=50g,即蒸发掉50g水也可以使溶液达到饱和。
由图可知,甲的溶解度随温度的升高而增加,故可降低温度,使溶液达到饱和,故填:加入甲物质30g或蒸发50g水或降低温度;
(4)从溶解度曲线可以看出:t3℃时,甲、乙、丙三种物质的溶解度的由大到小的顺序是甲>乙>丙。

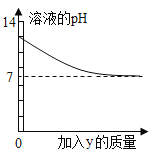
【题目】烧杯中盛有x溶液,逐滴加入(或通入)y物质,烧杯内液体的pH变化如图所示。则符合该变化的一组物质是( )
x | y | |
A | NaOH溶液 | 稀HCl(过量) |
B | Ca(OH)2 | CO2(适量) |
C | 稀H2SO4 | Ba(NO3)2溶液 |
D | 稀HCl | H2O |
A.AB.BC.CD.D
【题目】有一种石灰石样品(杂质既不溶于水也不与盐酸反应),某化学兴趣小组为了测定该石灰石样品中碳酸钙的质量分数,取12克样品放入烧杯中,再取100克稀盐酸分5次加入烧杯中,充分反应后,测得实验数据如下:
第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
加入稀盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
反应后烧杯内物质的质量(g) | 30.9 | 49.8 | 68.7 | 87.6 | 107.6 |
计算:(1)碳酸钙中各元素的质量比_____。
(2)完全反应时,生成二氧化碳的总质量为_____克。
(3)样品中碳酸钙的质量质量分数。_____(计算结果精确到0.1%)