题目内容
【题目】为研究酸的化学性质,进行如图实验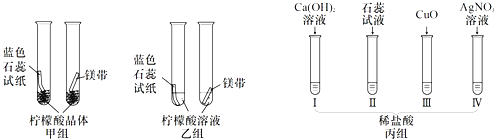 C
C
(1)甲组实验中两支试管均无明显现象,乙组中的现象是:蓝色石蕊试纸变 , 镁带表面有 . 这两组实验说明 .
(2)丙组实验试管Ⅳ中发生反应的化学方程式是
(3)丙组实验中无明显现象的是(填试管编号),下列实验不能证明两者发生了反应的是 .
a、测定加入另一反应物前后温度的变化:温度升高
b、测定加入另一反应物前后溶液pH的变化:pH变大
c、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红
d、取该试管实验后的剩余溶液滴加碳酸钠,无气泡
(4)为了验证盐酸具有酸的通性,丙组中还需添加的实验是:向稀盐酸中加入 .
【答案】
(1)红色;气泡产生;酸的很多反应通常要在水溶液中才能完成
(2)HCl+AgNO3=AgCl↓+HNO3
(3)Ⅰ;b
(4)活泼金属
【解析】(1)乙组中柠檬酸溶解,可以电离出氢离子,具有酸的通性,蓝色石蕊试纸变红色,镁带表面有气泡产生.这两组实验说明酸的很多反应通常要在水溶液中才能完成;
(2)硝酸银与盐酸反应生成氯化银和硝酸,化学方程式为:HCl+AgNO3=AgCl↓+HNO3;
(3)A、向盐酸中加入氢氧化钙溶液后,混合溶液的温度升高,说明反应放出了热量,可以说明它们发生了反应,此项能证明;
B、测定加入另一反应物前后溶液pH的变化:pH变大,不能证明两者发生了反应,盐酸溶液被稀释,pH也变大,此项不能证明;
C、先向稀盐酸中滴加酚酞,再逐渐加入另一反应物,一段时间后溶液变红,说明前期加入的氢氧化钙溶液被反应掉,可以说明它们发生了反应,此项能证明;
D、取该试管实验后的剩余溶液滴加碳酸钠,无气泡,说明盐酸已被反应掉,可以说明它们发生了反应,此项能证明;
故选:B.
(4)酸的能与指示剂、活泼金属、金属氧化物、碱、某些盐等反应,图中已经包含指示剂、金属氧化物、碱、盐,所以为了验证盐酸具有酸的通性,丙组中还需添加的实验是:向稀盐酸中加入活泼金属.
故答案为:(1)红色;气泡产生;酸的很多反应通常要在水溶液中才能完成;(2)HCl+AgNO3=AgCl↓+HNO3;(3)Ⅰ;b(4)活泼金属(合理给分).
(1)指示剂、金属可以和酸液反应,但是不能与酸的固体反应,是因为酸的很多反应通常要在水溶液中才能完成;(2)硝酸银与盐酸反应生成氯化银和硝酸;(3)氢氧化钙与盐酸反应生成氯化钙和水没有明显现象;(4)根据酸的化学性质(能与活泼金属、金属氧化物、碱、碳酸盐等反应),据此进行分析解答.

【题目】一包白色固体中可能含有碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种.某小组为探究其成分进行如下实验: 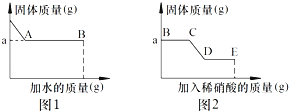
Ⅰ.取少量固体于烧杯中逐渐加水并不断搅拌,烧杯中固体质量随加入的水的质量变化如图1所示
Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞变红
Ⅲ.向实验Ⅰ所得的混合物中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示.
(1)CD段可观察到的现象是 , 从D到E的溶液的pH(填“增加”、“减小”、“不变”).
(2)根据上述实验得出原固体中一定有 .
(3)为进一步探究该白色固体成分,进行如下实验
步骤 | 现象 | 结论 |
取实验Ⅱ反应后的溶液于试管中, | 原固体中有氢氧化钠 | |
取实验Ⅱ反应后的溶液于试管中, |