题目内容
(2008?崇文区二模)黄铜是铜和锌的合金.向一定质量的黄铜样品中加入154.7g稀硫酸,恰好完全反应,产生0.2g氢气.(1)求所用稀硫酸的溶质质量分数
(2)除了可求出稀硫酸的溶质质量分数外,你还能求出的化学量有______.(填序号)
①锌的质量 ②铜的质量分数 ③锌的质量分数 ④硫酸锌的质量 ⑤硫酸溶液的体积 ⑥反应后溶液溶质质量分数.
【答案】分析:根据金属活动性强弱关系锌>氢>铜可知,把黄铜放入稀硫酸时,锌可与硫酸反应生成硫酸锌同时放出氢气;利用反应的化学方程式,由反应生成氢气的质量可计算消耗锌的质量、消耗硫酸的质量及生成硫酸锌的质量,然后利用硫酸质量与稀硫酸质量比还可计算出稀硫酸中硫酸的溶质质量分数;根据质量守恒定律,还可计算出反应后所得溶液的质量,因此还可计算反应后硫酸锌溶液的溶质质量分数.
解答:解:(1)设参加反应的硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.2g
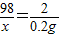 x=9.8g
x=9.8g
所用稀硫酸的溶质质量分数=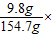 100%≈6.3%
100%≈6.3%
答:所用稀硫酸的溶质质量分数为6.3%;
(2)根据反应的化学方程式,还可以计算出锌的质量、硫酸锌的质量;但由于不知道黄铜的质量,因此不能计算出黄铜中铜的质量分数、锌的质量分数;由于不知道硫酸溶液的密度,因此也不能把硫酸溶液的质量转变为体积;根据质量守恒定律,反应后溶液质量可由参加反应锌的质量+所加稀硫酸的质量-放出氢气的质量而计算出来,因此,还可以计算出所加稀硫酸的溶质质量分数;
故答案为:①④⑥.
点评:反应的化学方程式可以表现出反应中各物质的质量关系,因此,利用反应的化学方程式可由反应中任一物质质量计算出反应中其它物质的质量.
解答:解:(1)设参加反应的硫酸的质量为x,
Zn+H2SO4=ZnSO4+H2↑
98 2
x 0.2g
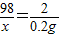 x=9.8g
x=9.8g所用稀硫酸的溶质质量分数=
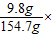 100%≈6.3%
100%≈6.3%答:所用稀硫酸的溶质质量分数为6.3%;
(2)根据反应的化学方程式,还可以计算出锌的质量、硫酸锌的质量;但由于不知道黄铜的质量,因此不能计算出黄铜中铜的质量分数、锌的质量分数;由于不知道硫酸溶液的密度,因此也不能把硫酸溶液的质量转变为体积;根据质量守恒定律,反应后溶液质量可由参加反应锌的质量+所加稀硫酸的质量-放出氢气的质量而计算出来,因此,还可以计算出所加稀硫酸的溶质质量分数;
故答案为:①④⑥.
点评:反应的化学方程式可以表现出反应中各物质的质量关系,因此,利用反应的化学方程式可由反应中任一物质质量计算出反应中其它物质的质量.

练习册系列答案
相关题目
(2008?崇文区二模)小刚做中和反应实验时,将稀盐酸滴入氢氧化钠溶液中,看到有气泡产生.是不是拿错了药品?小刚经检验确认没有拿错药品,而是氢氧化钠溶液变质了.
【分析】氢氧化钠溶液变质的原因是______.
【提出问题】该氢氧化钠溶液是全部变质还是部分变质?
【查询资料】1.已知反应:BaCl2+Na2CO3═2NaCl+BaCO3↓
2.部分盐溶液的pH如下表:
【实验设计】小刚依据查询的资料设计实验步骤,请你帮他补充完整.
【实验结论】通过实验,小刚检验出该氢氧化钠溶液只是部分变质.
【进一步实验】小刚用变质的溶液制取不含杂质的氢氧化钠溶液,继续完成中和反应实验.他设计如图所示的实验方案.

(1)写出步骤①发生反应的化学方程式______;
(2)步骤①中滴加适量溶液A后的操作是______;
(3)步骤③判断盐酸与氢氧化钠恰好完全反应的实验现象是______.
【分析】氢氧化钠溶液变质的原因是______.
【提出问题】该氢氧化钠溶液是全部变质还是部分变质?
【查询资料】1.已知反应:BaCl2+Na2CO3═2NaCl+BaCO3↓
2.部分盐溶液的pH如下表:
| 盐溶液 | NaCl | Na2CO3 | BaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加足量的氯化钡溶液,并不断振荡. | 说明原来溶液中,一定含有的溶质是碳酸钠. | |
| (2)向步骤(1)充分反应后的溶液中滴加. | 说明原来溶液中,还一定含有. |
【进一步实验】小刚用变质的溶液制取不含杂质的氢氧化钠溶液,继续完成中和反应实验.他设计如图所示的实验方案.

(1)写出步骤①发生反应的化学方程式______;
(2)步骤①中滴加适量溶液A后的操作是______;
(3)步骤③判断盐酸与氢氧化钠恰好完全反应的实验现象是______.
 (2008?崇文区二模)如图是某试剂瓶上已经部分被污损和腐蚀的标签.小明想探究其成分,他取一支洁净的试管,加入少量试剂瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
(2008?崇文区二模)如图是某试剂瓶上已经部分被污损和腐蚀的标签.小明想探究其成分,他取一支洁净的试管,加入少量试剂瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( ) (2008?崇文区二模)如图是某试剂瓶上已经部分被污损和腐蚀的标签.小明想探究其成分,他取一支洁净的试管,加入少量试剂瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
(2008?崇文区二模)如图是某试剂瓶上已经部分被污损和腐蚀的标签.小明想探究其成分,他取一支洁净的试管,加入少量试剂瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )