题目内容
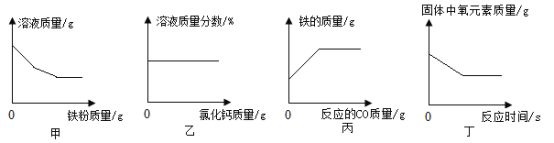
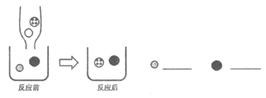
【题目】某学习小组设计了图的实验,用稀盐酸测定100g被部分氧化的铜样品中铜的含量。请计算:

(1)m=________。
(2)所用稀盐酸中溶质的质量分数_____。
【答案】92 7.3%
【解析】
(1)根据反应前后,参见反应的各物质的质量等于反应后生成的各物质的质量总和进行分析;
(2)根据氧化铜的质量结合氧化铜和稀盐酸反应的方程式计算氯化氢的质量,进而计算溶质的质量分数。
解:(1)根据质量守恒定律可知,滤渣的质量=300g-208g=92g;
(2)样品中含有氧化铜的质量为(100-92)g=8g,设稀盐酸溶液中含有的HCl的质量为x,
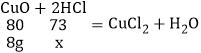
![]()
x=7.3g,
盐酸溶液中溶质的质量分数为![]() ×100%=7.3%;
×100%=7.3%;
答:盐酸中溶质的质量分数为7.3%。

练习册系列答案
相关题目