题目内容
镁条在空气中燃烧,不仅生成氧化镁,还有少量镁与氮气化合生成氮化镁(Mg3N2).(1)请你写出镁条燃烧生成氧化镁的化学反应方程式
(2)若有24克镁在空气中完全燃烧,则所得产物的总质量m
分析:(1)根据反应物与生成物写化学方程式,注意写,查,配,注;
(2)根据Mg在空气中燃烧与氧气和氮气反应的情况:
如果全部生成MgO,依据方程式计算出氧化镁的质量;
如果全部生成Mg3N2,依据方程式计算出氮化镁的质量,实际情况介于两者之间,即可解答本题.
(2)根据Mg在空气中燃烧与氧气和氮气反应的情况:
如果全部生成MgO,依据方程式计算出氧化镁的质量;
如果全部生成Mg3N2,依据方程式计算出氮化镁的质量,实际情况介于两者之间,即可解答本题.
解答:解:(1)根据反应物与生成物,镁条燃烧只生成氧化镁的化学方程式为:2Mg+O2
2MgO;
故答案为:2Mg+O2
2MgO;
(2)根据Mg在空气中燃烧只考虑与氧气和氮气反应的情况:
如果全部生成MgO,2Mg+O2
2MgO
2×24 2×40
24 m 则m=40g
如果全部生成Mg3N2,3Mg+N2
Mg3N2
3×24 100
24 m
则 m=33.3g
实际情况介于两者之间,所以m<40g;
故答案为:<
| ||
故答案为:2Mg+O2
| ||
(2)根据Mg在空气中燃烧只考虑与氧气和氮气反应的情况:
如果全部生成MgO,2Mg+O2
| ||
2×24 2×40
24 m 则m=40g
如果全部生成Mg3N2,3Mg+N2
| ||
3×24 100
24 m
则 m=33.3g
实际情况介于两者之间,所以m<40g;
故答案为:<
点评:本题主要考查有关化学方程式的计算,难度较大.关键是找到产物的质量介于产物全部为氧化镁的质量和产物全部为氮化镁的质量之间.

练习册系列答案
相关题目
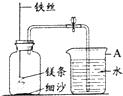 12、某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
12、某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.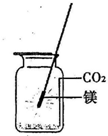 镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是
镁在空气中燃烧时既会与氧气反应生成氧化镁,同时也会与氮气反应生成氮化镁.已知氮化镁是黄绿色固体,根据镁条在空气中燃烧时的现象可知:在这样的条件下,镁更易与 O2 化合,理由是