题目内容
【题目】空气中氧气含量测定的再认识。
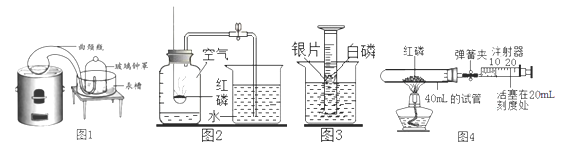
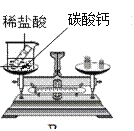
【经典赏析】拉瓦锡用定量的方法研究了空气的成分(装置如图1),通过该实验拉瓦锡得出了空气是由氧气和____________(填物质名称)组成的,其中氧气约占空气总体积的1/5。
【实验回顾】
(1)实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),兴趣小组用该方法测出的氧气含量常常远低于1/5。其原因可能是:装置漏气;红磷量不足,装置内氧气有剩余;_______ ;…
(2)由于红磷在空气中点燃后才放入集气瓶内,实验缺陷:①测定结果不准确;②____________。
【提出问题】能否设计一套实验装置以解决上述缺陷?
【实验改进】
改进一:兴趣小组同学,设计了如图3所示装置:用一个100mL量筒倒扣在水中,使量筒内外液面均位于40mL处,量筒内浮着一个贴有银片的小木块,银片上放有足量白磷,将整套装置置于垫有_________(填仪器名称)的铁架台的铁圈上加热。一会儿,白磷发生燃烧,量筒内液面上升,向烧杯内加水直至量筒内外液面相平,读出此时液面所对刻度。
(3)放白磷的平板用银做的原因是:银的_____________(填物理性质)性好,易将白磷温度升高,且化学性质稳定;
(4)最终,液面大约位于量筒刻度______mL处;白磷燃烧的文字表达式为_____________。
改进二:兴趣小组同学又进行了大胆改进,设计图4(选用容积为40mL的的试管作反应容器,注射器活塞初始位置为20mL处,注射器空间为20mL,活塞与内壁摩擦力及连接管空间容积忽略不计)实验方案进行,收到了良好的效果。
(5)兴趣小组同学装配好图4装置,确认气密性良好后,将弹簧夹松开,直接给足量的红磷加热,红磷燃烧后,一开始活塞的运动方向为_____________,反应完全并冷却后,注射器活塞最终将停留在约为_______mL(填整数)刻度处。
【交流反思】
(6)对照图2,改进后的实验装置有何优点_____________(答一点即可)。
【答案】 氮气 未等冷却就打开弹簧夹 污染空气 (合理答案皆可) 石棉网 导热 32 磷+氧气 ![]() 五氧化二磷或磷+氧气
五氧化二磷或磷+氧气 ![]() 五氧化二磷 向右移动 8 减少实验误差(不污染环境或便于读数)(其他合理答案给分)
五氧化二磷 向右移动 8 减少实验误差(不污染环境或便于读数)(其他合理答案给分)
【解析】拉瓦锡用定量的方法研究了空气的成分,通过该实验得出了空气是由氧气和氮气组成的;(1) 红磷燃烧的方法测定空气中氧气的含量常常远低于1/5,其原因可能是:装置漏气;红磷量不足,装置内氧气有剩余,未等冷却就打开弹簧夹; (2) 红磷在空气中生成五氧化二磷有毒并放出热量,点燃后才放入集气瓶内会赶走瓶内的一部分空气,也会污染空气;给烧杯加热时必须垫石棉网;(3) 放白磷的平板用银做的原因是利用银的导热性好,易将白磷温度升高,且化学性质稳定;(4) 足量白磷燃烧会消耗完装置内的氧气并生成五氧化二磷,即气体体积减少8 mL,故填:32,磷+氧气![]() 五氧化二磷;(5) 兴趣小组同学装配好仪器并确认气密性良好后.第一组同学将弹簧夹夹紧橡皮管,给足量的红磷加热,燃烧结束待试管冷却后松开弹簧夹,由于只消耗了试管内的氧气,所以氧气的体积是40mL的五分之一,为8mL,所以注射器活塞将从20mL刻度处前移到约为 12mL刻度处才停止.第二组同学将弹簧夹松开,直接给足量的红磷加热,由于反应放热,所以红磷燃烧后活塞运动方向为先向右,然后由于氧气消耗,且温度降低,所以活塞最后向左.由于装置内氧气均被消耗,所以氧气的体积为60mL的五分之一,为12mL,所以反应完全并冷却后,注射器活塞最终将停留在约为 8mL刻度处;(6) 对照图2,改进后的实验装置优点:由于一直在密闭环境反应,所以不污染环境,由于注射器有刻度,所以变化读数,所以有点有减少实验误差、不污染环境或便于读数等。
五氧化二磷;(5) 兴趣小组同学装配好仪器并确认气密性良好后.第一组同学将弹簧夹夹紧橡皮管,给足量的红磷加热,燃烧结束待试管冷却后松开弹簧夹,由于只消耗了试管内的氧气,所以氧气的体积是40mL的五分之一,为8mL,所以注射器活塞将从20mL刻度处前移到约为 12mL刻度处才停止.第二组同学将弹簧夹松开,直接给足量的红磷加热,由于反应放热,所以红磷燃烧后活塞运动方向为先向右,然后由于氧气消耗,且温度降低,所以活塞最后向左.由于装置内氧气均被消耗,所以氧气的体积为60mL的五分之一,为12mL,所以反应完全并冷却后,注射器活塞最终将停留在约为 8mL刻度处;(6) 对照图2,改进后的实验装置优点:由于一直在密闭环境反应,所以不污染环境,由于注射器有刻度,所以变化读数,所以有点有减少实验误差、不污染环境或便于读数等。

【题目】人教版化学教材九年级上册“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
实验步骤 | 实验现象 |
I.分别取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 |
|
IV.分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
|
【实验结论】
(1)A中产生的气体是______________;
(2)实验II、III证明:氧化铁的____________和 ___________在反应前后均没有发生变化,可以作为过氧化氢分解的催化剂;
(3)写出氧化铁催化过氧化氢分解的文字表达式__________________________。
【实验评价】
(4)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是__________。
【实验拓展】
(5)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是(___________)
A.MnO2只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物