题目内容
(3分)由铁元素和氧元素组成的铁的某种氧化物中,铁和氧的质量比为21:8,该氧化物的相对分子质量为232,试通过计算确定该氧化物的化学式。
Fe3O4
分析:根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析解答.
解:设铁元素和氧元素组成的铁的某种氧化物的化学式为:FexOy,依据铁和氧的质量比为21:8,可得
56x:16y=21:8 解答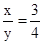
由此可知该氧化物中铁原子与氧原子的个数比为 3:4;
可知 56x+16y=232,
得x=3 y=4
因此可确定该氧化物的化学式为:Fe3O4.
答:该氧化物的化学式为:Fe3O4,
点评:本题考查学生根据化合物中各元素质量比进行分析求物质化学式的解题能力及灵活应用的能力.
解:设铁元素和氧元素组成的铁的某种氧化物的化学式为:FexOy,依据铁和氧的质量比为21:8,可得
56x:16y=21:8 解答
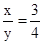
由此可知该氧化物中铁原子与氧原子的个数比为 3:4;
可知 56x+16y=232,
得x=3 y=4
因此可确定该氧化物的化学式为:Fe3O4.
答:该氧化物的化学式为:Fe3O4,
点评:本题考查学生根据化合物中各元素质量比进行分析求物质化学式的解题能力及灵活应用的能力.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
