题目内容
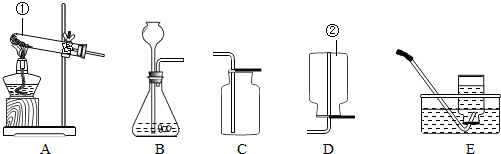
 如图为实验室制取气体的常用发生装置.回答下列问题:
如图为实验室制取气体的常用发生装置.回答下列问题:(1)仪器a的名称是 .
(2)实验室可用A装置制取氧气,反应的化学方程式为 ,收集氧气可用 法.
(3)用过氧化氢制取氧气,反应的发生装置应选择 .检验氧气是否收集满的方法是 .
(4)盐酸是氯化氢的水溶液.实验室用氯化钠和浓硫酸混合加热制取氯化氢气体,反应的化学方程式为 .
【答案】分析:(1)依据常用仪器回答;
(2)A装置是用加热固体的方法制取氧气,且试管口有棉花,故是用加热高锰酸钾的方法制取氧气,据反应原理书写方程式,并据氧气的密度和溶解性选择收集方法;
(3)依据反应物的状态和反应条件选择发生装置,检验氧气是否收集满将带火星的木条放于集气瓶口,观察是否复燃进行判断;
(4)依据复分解反应的原理推测生成物,并据方程式的书写方法书写反应方程式.
解答:解:(1)仪器a是试管;
(2)A装置是用加热固体的方法制取氧气,且试管口有棉花,故是用加热高锰酸钾的方法制取氧气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4 K2MnO4+MnO2+O2↑;氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集氧气;
K2MnO4+MnO2+O2↑;氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集氧气;
(3)过氧化氢在二氧化锰的催化作用下分解生成氧气,反应不需加热,故选发生装置B;检验氧气是否收集满将带火星的木条放于集气瓶口,观察是否复燃进行判断;
(4)依据复分解反应的特点:两种化合物相互交换成分生成另外两种化合物,可知氯化钠和浓硫酸混合加热制取氯化氢气体的同时生成硫酸钠,方程式是:2NaCl+H2SO4(浓) Na2SO4+2HCl↑;
Na2SO4+2HCl↑;
故答案为:(1)试管;
(2)2KMnO4 K2MnO4+MnO2+O2↑; 排水法或向上排空气;
K2MnO4+MnO2+O2↑; 排水法或向上排空气;
(3)B; 将带火星的木条放在瓶口,木条复燃,证明已经收集满了;
(4)2NaCl+H2SO4(浓) Na2SO4+2HCl↑.
Na2SO4+2HCl↑.
点评:依据反应物的状态和反应条件选择发生装置,依据气体的密度和选择收集装置,并掌握方程式的书写、检验氧气是否收集满的方法是解答此题的关键.
(2)A装置是用加热固体的方法制取氧气,且试管口有棉花,故是用加热高锰酸钾的方法制取氧气,据反应原理书写方程式,并据氧气的密度和溶解性选择收集方法;
(3)依据反应物的状态和反应条件选择发生装置,检验氧气是否收集满将带火星的木条放于集气瓶口,观察是否复燃进行判断;
(4)依据复分解反应的原理推测生成物,并据方程式的书写方法书写反应方程式.
解答:解:(1)仪器a是试管;
(2)A装置是用加热固体的方法制取氧气,且试管口有棉花,故是用加热高锰酸钾的方法制取氧气,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
 K2MnO4+MnO2+O2↑;氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集氧气;
K2MnO4+MnO2+O2↑;氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集氧气;(3)过氧化氢在二氧化锰的催化作用下分解生成氧气,反应不需加热,故选发生装置B;检验氧气是否收集满将带火星的木条放于集气瓶口,观察是否复燃进行判断;
(4)依据复分解反应的特点:两种化合物相互交换成分生成另外两种化合物,可知氯化钠和浓硫酸混合加热制取氯化氢气体的同时生成硫酸钠,方程式是:2NaCl+H2SO4(浓)
 Na2SO4+2HCl↑;
Na2SO4+2HCl↑;故答案为:(1)试管;
(2)2KMnO4
 K2MnO4+MnO2+O2↑; 排水法或向上排空气;
K2MnO4+MnO2+O2↑; 排水法或向上排空气;(3)B; 将带火星的木条放在瓶口,木条复燃,证明已经收集满了;
(4)2NaCl+H2SO4(浓)
 Na2SO4+2HCl↑.
Na2SO4+2HCl↑.点评:依据反应物的状态和反应条件选择发生装置,依据气体的密度和选择收集装置,并掌握方程式的书写、检验氧气是否收集满的方法是解答此题的关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目