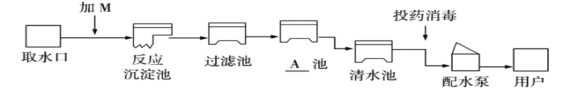
题目内容
【题目】分析一:化学实验中的一些现象可借助压强的变化来分析。
实验内容 | 实验现象 | 实验分析 |
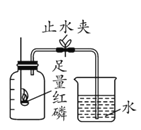
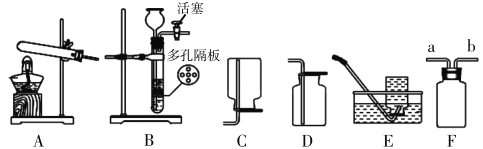
A.空气中氧气含量的测定 | 待装置冷却后打开止水夹,水进入集气瓶,约占集气瓶容积的五分之一 | 水进入集气瓶约占集气瓶容积五分之一的原因是_________ |
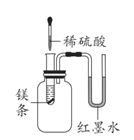
B.镁条反应实验 | 向试管中加人稀硫酸,可观察到U形管中红墨水____________________(填“左”或“右”,下同)低___________________________高 | 出现此现象的原因是镁与稀硫酸反应放热,使瓶内压强增大 |
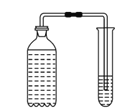
C.将汽水中的二氧化碳通入含紫色石蕊 | 振荡汽水瓶,可观察到试管中的紫色石蕊试液变红 | 紫色石蕊试液变红的原因是____________________________(用化学方程式表示) |
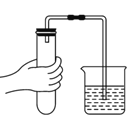
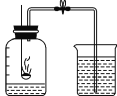
D.检查装置气密性 | 若装置气密性良好,则出现的现象为_____________________________________。 | 出现此现象的原因是用手捂住试管时,试管内温度升高,压强增大,松开手后,试管内温度降低,压强减小 |
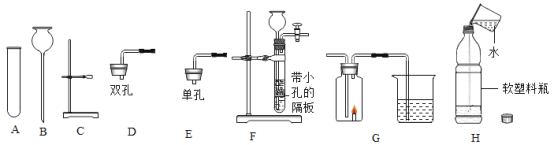
分析二:如图所示,用胶头滴管向装有固体的广口瓶中滴加液体,使气球变大,请从不同反应类型的角度大胆猜想使用的固体和液体分别是(请写出三种组合):

猜想一:__________________________________________________。
猜想二:__________________________________________________。
猜想三:__________________________________________________。
【答案】足量红磷燃烧消耗尽了瓶内的氧气,生成物为固体,导致瓶内压强减小,在大气压的作用下,水进入集气瓶中,由于氧气约占空气总体积的五分之一,所以进入的水也约占瓶内容积的五分之一 左 右 ![]() 导管口有气泡产生,松开手后导管中形成一段稳定的水柱 氧化钙和水(其他合理答案均可) 镁和稀硫酸(其他合理答案均可) 碳酸钙和稀盐酸(其他合理答案均可)
导管口有气泡产生,松开手后导管中形成一段稳定的水柱 氧化钙和水(其他合理答案均可) 镁和稀硫酸(其他合理答案均可) 碳酸钙和稀盐酸(其他合理答案均可)
【解析】
分析一:A、足量红磷燃烧消耗尽了瓶内的氧气,且生成物为固体,导致瓶内压强减小,在大气压的作用下,水进入集气瓶中,由于氧气约占空气总体积的五分之一,所以进入的水也约占瓶内容积的五分之一;
B、镁与稀硫酸反应放出大量的热,使瓶内温度升高,压强变大,所以U形管中的液面左低右高;
C、振荡汽水瓶时,其中的二氧化碳逸出进人紫色石蕊试液中,二氧化碳与水反应生成碳酸,碳酸显酸性,能使紫色石蕊试液变红色,反应的化学方程式为![]() ;
;
D、用微热法检查装置气密性时,如果装置气密性良好,用手捂住试管外壁,试管内气体温度升高,压强增大,所以导管口会产生气泡,松手后,由于试管内温度下降,造成试管内压强减小,所以导管内液面上升,并形成一段稳定的水柱;
分析二:气球变大,说明瓶内压强增大,瓶内温度升高或气体增加都会使瓶内压强增大,从化合反应角度:氧化钙与水反应放出热量,温度升高,瓶内压强增大,可使气球体积增大;从置换反应角度:活动性较强的金属与稀盐酸或稀硫酸反应生成气体,如镁与稀硫酸反应,放出氢气,内部气体增多,压强增大,气球体积变大;从复分解反应角度:碳酸盐与稀盐酸或稀硫酸反应生成气体,如碳酸钙与稀盐酸反应,生成二氧化碳,内部气体增多,压强变大,气球变大;从分解反应角度:过氧化氢溶液在二氧化锰催化下分解生成氧气,内部气体增多,压强增大,气球体积变答,因此可以从多个方面进行猜想,只要回答答案合理即可。

【题目】请参与下列探究实验:
(实验探究)
步骤 | 实验操作 | 实验现象 | 结论或解释 |
(1) | 用玻棒分别蘸取95%的酒精、蒸馏水置于火焰上。 | 酒精_______,蒸馏水_______。 | 结论:酒精是可燃物,水不是可燃物。 |
(2) | 在铁片两端放大小相同的硬纸片、乒乓球碎片,在铁片中间加热。 | 乒乓球碎片先燃烧、硬纸片后燃烧。 | 结论:乒乓球碎片的________比硬纸片的低。 |
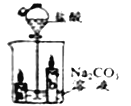
(3) | 在右图中打开分液漏斗的旋塞 | ①溶液中产生气泡;②蜡烛火焰a_____填“先于”“后于”)b熄灭。 | 现象②的原因是:CO2不助燃;___________。 |
(4) | 用大烧杯罩住高低两支点燃的蜡烛。 | ①烧杯底部变黑;②蜡烛火焰d比c先熄灭。 | CO2不助燃,蜡烛不完全燃烧;d先熄灭的原因是:_______。 |
(拓展)堆积的面粉不容易点燃,即使少量点燃也只是小火燃烧;如果把面粉撒向空中遇火星可能会发生爆炸。“小火燃烧”和“发生爆炸”的原因分别是:_______________。