题目内容
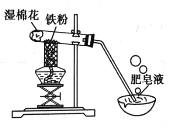
【题目】实验室用碱式碳酸铜[化学式:Cu2(OH)2CO3]制备氧化铜并检验其产物,装置如下:
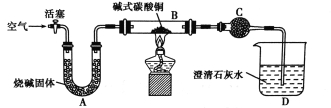
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录B中固体质量变化如下表,在t3时停止加热。

(1)步骤一通入空气的目的是__________________________。
(2)C中试剂是_______(填名称);A的作用是吸收空气中的_______(填名称)。
(3)选择t3时停止加热的理由是________________________。
(4)B中发生反应的化学方程式为:_____________________________。
【答案】(1)排出硬质玻璃管B中的水蒸气和二氧化碳,防止干扰实验结果
(2)无水硫酸铜 水蒸气
(3)t3时与t2时相比,固体质量不再改变,说明碱式碳酸铜已完全分解
(4)Cu2(OH)2CO3=加热=2CuO+H2O+CO2↑
【解析】
试题分析:(1)反应容器内存有空气,需让其流动以除去水蒸气和二氧化碳;
(2)为检测是否有水蒸气,可用无水硫酸铜,其遇水生成蓝色的5水硫酸铜;能吸水和除去二氧化碳,以避免对实验的干扰;
(3)固体质量不再变化时,可以认为碱式碳酸铜完全分解,t2,t3时固体质量不再改变,所以选择t3时停止加热的理由是:固体质量不再减少,证明碱式碳酸铜已经完全分解;

练习册系列答案
相关题目