题目内容
(2011?武清区一模)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如下: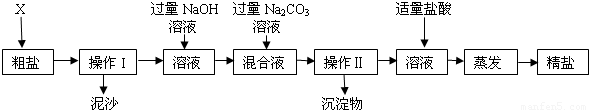
根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的物质X是______;
(2)操作Ⅰ中要用到的仪器有玻璃棒,它作用是____________;
(3)在实验过程中加入过量的氢氧化钠溶液,其实验目的是______;
(4)在蒸发操作时,应把所得溶液倒入蒸发皿中,把蒸发皿放在铁架台的铁圈上,用______
______,待蒸发皿中出现较多固体时停止加热,利用余热把剩余的水蒸干,冷却,即可得到纯净的精盐;
(5)实验所得的精盐的质量______(填“大于”、“小于”或“等于”)粗盐中氯化钠的质量,原因是______.
【答案】分析:(1)根据粗盐的提纯需要将其配成溶液才能进行,
(2)玻璃棒在溶解时可以加速溶解,在过滤时起引流的作用,
(3)氢氧化钠可以将水中的氢离子转化为沉淀而得到净水的目的,
(4)蒸发过程中需要酒精灯提供热源并用玻璃棒不断搅拌,
(5)在过滤和转移固体时会造成氯化钠损耗,但是过程中生成的氯化钠会更多一些..
解答:解:(1)海水晾晒得到的粗盐是固体,要进行提纯,需要先配成溶液,故答案为:水.
(2)用玻璃棒搅拌可以加快水的流动,加速了固体溶解,过滤时,玻璃棒引流防止液滴外溅,故答案为:加速食盐溶解,过滤引流.
(3)加入过量的氢氧化钠,氢氧根离子可以和镁离子转化为氢氧化镁沉淀而将镁离子除去,故答案为:将镁离子全部沉淀.
(4)在进行蒸发操作时,需要用到酒精灯提供热源,用到玻璃棒不断搅拌,防止液滴外溅,故答案为:酒精灯加热,玻璃棒不断搅拌.
(5)在粗盐提纯的过程中,由于生成了氯化钠,导致质量增减.故答案为:大于,在粗盐提纯的过程中生成了氯化钠.
点评:本题从多个角度对氯化钠的提纯实验进行了全面考察,灵活性强.
(2)玻璃棒在溶解时可以加速溶解,在过滤时起引流的作用,
(3)氢氧化钠可以将水中的氢离子转化为沉淀而得到净水的目的,
(4)蒸发过程中需要酒精灯提供热源并用玻璃棒不断搅拌,
(5)在过滤和转移固体时会造成氯化钠损耗,但是过程中生成的氯化钠会更多一些..
解答:解:(1)海水晾晒得到的粗盐是固体,要进行提纯,需要先配成溶液,故答案为:水.
(2)用玻璃棒搅拌可以加快水的流动,加速了固体溶解,过滤时,玻璃棒引流防止液滴外溅,故答案为:加速食盐溶解,过滤引流.
(3)加入过量的氢氧化钠,氢氧根离子可以和镁离子转化为氢氧化镁沉淀而将镁离子除去,故答案为:将镁离子全部沉淀.
(4)在进行蒸发操作时,需要用到酒精灯提供热源,用到玻璃棒不断搅拌,防止液滴外溅,故答案为:酒精灯加热,玻璃棒不断搅拌.
(5)在粗盐提纯的过程中,由于生成了氯化钠,导致质量增减.故答案为:大于,在粗盐提纯的过程中生成了氯化钠.
点评:本题从多个角度对氯化钠的提纯实验进行了全面考察,灵活性强.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目