题目内容
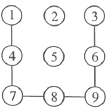
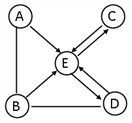
【题目】下面是几种粒子的结构示意图:
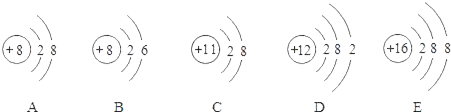
(1)A~E共有_____种元素;
(2)表示原子的粒子有_____;
(3)表示阴离子的有_____;
(4)表示阳离子的有_____;
(5)表示相对稳定结构的是_____;
(6)在化学反应中易得到电子的粒子是_____;
(7)下列几种物质是按氯元素化合价规律排列为KC1、_____、HClO、KClO3、HClO4,空格内物质应是_____。
A NaCl B NaClO C Cl2 D HClO3
【答案】3 BD AE C ACE B Cl2 C
【解析】
(1)据图可以看出,A~E共有四种元素;
(2)B和D的核内质子数=核外电子数,表示的是原子,表示原子的粒子有BD,故填:BD;
(3)A和E的核内质子数<核外电子数,表示的是阴离子;
(4)C的核内质子数>核外电子数,表示的是阳离子;
(5)A、C、E的最外层电子数是8,达到了稳定结构;
(6)B的最外层电子数大于4,在化学反应中易得到电子;
(7)在化合物中正负化合价代数和为零,钾元素的化合价为+1价,氢元素的化合价为+1价,钠元素的化合价为+1价,氧元素的化合价为﹣2价,则:KCl中氯元素的化合价为﹣1价;HClO中氯元素的化合价为+1价;KClO3中氯元素的化合价为+5价;HClO4中氯元素的化合价为+7价;则氯元素的化合价是按照从低到高的顺序排列的,空中氯元素的化合价为在﹣1到+1之间;
A、钠元素显+1价,NaCl中氯元素的化合价为﹣1价,不符合排列规律;
B、钠元素显+1价,氧元素的化合价为﹣2价,NaClO中氯元素的化合价为:+1价,不符合排列规律;
C、根据单质中元素的化合价为0,Cl2属于单质,故氯元素的化合价为0,符合排列规律;
D、氢元素的化合价为+1价,氧元素的化合价为﹣2价,HClO3中氮元素的化合价为:+5价,不符合排列规律。

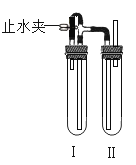
【题目】质量守恒定律是化学反应遵循的普遍规律。
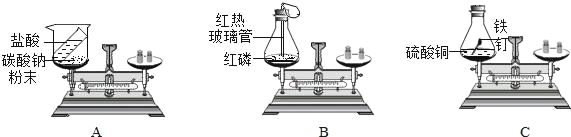
(1)上述实验方案中,不能用于验证质量守恒定律的是_____(填字母序号),其原因是_____。
(2)某反应在点燃的条件下发生,涉及甲、乙、丙和丁四种物质,它们的微观示意图和反应前后的质量如下表所示。
物质序号 | 甲 | 乙 | 丙 | 丁 |
|
微观 示意图 |
|
|
|
| |
反应前质量/g | 68 | 100 | 1 | 0 | |
反应后质量/g | 0 | x | y | z |
①丁的化学式为_____。
②表中的四种物质中,含氧元素的化合物是_____(填物质序号)。
③上述反应的化学方程式为_____。
④一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是_____(填字母序号)。
A x+y+z=169 B y+z=168
C (100﹣x):z=32:64 D (100﹣x):(y﹣1)=8:3