题目内容
 金属材料在人类活动中已得到越来越广泛的应用.
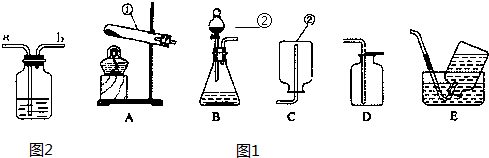
金属材料在人类活动中已得到越来越广泛的应用.(1)利用如图所示的实验探究,可获得什么结论
(2)很多金属制品表面镀铝防锈,其原因是什么?
(3)利用硫酸铜、石灰水配制农药波尔多液,不宜在铁制容器进行.请用化学方程式
说明原因.
考点:合金与合金的性质,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据如图所示的实验探究,黄铜片能在纯铜片上刻划出痕迹,进行分析解答.
(2)根据铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,进行分析解答.
(3)铁的活动性比铜强,铁和硫酸铜溶液反应会生成硫酸亚铁溶液和铜,故不宜在铁制容器配制农药波尔多液,据此进行分析解答.
(2)根据铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,进行分析解答.
(3)铁的活动性比铜强,铁和硫酸铜溶液反应会生成硫酸亚铁溶液和铜,故不宜在铁制容器配制农药波尔多液,据此进行分析解答.
解答:解:(1)由如图所示的实验探究,黄铜片能在纯铜片上刻划出痕迹,说明合金比组成它的纯金属的硬度大.
(2)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的金属被氧化,因此很多金属制品表面镀铝防锈.
(3)铁的活动性比铜强,铁和硫酸铜溶液反应会生成硫酸亚铁溶液和铜,故不宜在铁制容器配制农药波尔多液,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为:(1)合金比组成它的纯金属的硬度大;(2)铝能与氧气形成致密的氧化铝薄膜,阻止内部金属氧化;(3)Fe+CuSO4═Cu+FeSO4.
(2)铝能与空气中氧气反应在其表面生成一层致密的氧化铝薄膜,防止内部的金属被氧化,因此很多金属制品表面镀铝防锈.
(3)铁的活动性比铜强,铁和硫酸铜溶液反应会生成硫酸亚铁溶液和铜,故不宜在铁制容器配制农药波尔多液,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为:(1)合金比组成它的纯金属的硬度大;(2)铝能与氧气形成致密的氧化铝薄膜,阻止内部金属氧化;(3)Fe+CuSO4═Cu+FeSO4.
点评:本题难度不大,掌握合金的特征、金属的化学性质、化学方程式的书写方法是正确解答本题的关键.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
居里夫人是一位献身科学的杰出女性,在1906年她发现了放射性元素镭,并测出镭的中子数为138,相对原子质量为226.镭原子核外电子数为( )
| A、88 | B、138 |
| C、80 | D、314 |
下列溶液中通入或加入括号中的物质,能使溶液pH明显减小的是( )
| A、澄清石灰水(二氧化碳) |
| B、氢氧化钠(稀硫酸) |
| C、氢氧化钡(硫酸钠) |
| D、稀盐酸(碳酸钠) |
下列关于物质的鉴别的描述错误的是( )
| A、用带火星木条是否复燃检验氧气 |
| B、用燃着的木条是否熄灭检验二氧化碳 |
| C、用燃着木条点燃且火焰呈淡蓝色,罩在火焰上方冷而干燥的烧杯内壁有水雾检验氢气 |
| D、用观察或者品尝味道的方法确定无色无味的液体就是水 |
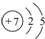 ,氮原子的最外层上的电子数为
,氮原子的最外层上的电子数为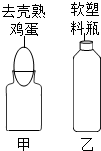 老师在课堂上表演了“瓶吞鸡蛋”的魔术,如图甲所示,老师把集气瓶“处理”一下后,把去壳熟鸡蛋放在了集气瓶口,一会儿鸡蛋就“自动”挤进集气瓶中.根据你学的知识解释鸡蛋“自动”挤进集气瓶中的原因:
老师在课堂上表演了“瓶吞鸡蛋”的魔术,如图甲所示,老师把集气瓶“处理”一下后,把去壳熟鸡蛋放在了集气瓶口,一会儿鸡蛋就“自动”挤进集气瓶中.根据你学的知识解释鸡蛋“自动”挤进集气瓶中的原因: