题目内容
氢氧化铜固体受热分解能得到两种氧化物,一种为固体,另一种是无色液体。某化学活动小组为确定这种固体产物是什么,进行了如下探究活动。
《假设》:生成的固体产物 ①可能是氧化亚铜(Cu2O)(红色) ;
②可能是 。
《设计实验》:小明用氢氧化钠溶液与硫酸铜溶液
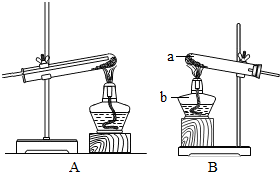
反应制得氢氧化铜,放入试管中,使其在加热条件下分解(如下图),观察到蓝色粉末逐渐变成黑色。

请指出仪器名称:a ,b 。
《推测结论》:猜想______成立。
《形成结论》:写出氢氧化铜受热分解的化学方程式:_______________________________。
《查阅资料》知:(1)此黑色固体可用氢气还原,则小明选择下列________装置进行实验;
(2)已知Cu2O有如下性质:Cu2O+H2SO4==Cu+CuSO4+H2O,在用氢气还原黑色固体后得到的铜中常混有少量Cu2O,取此Cu和Cu2O的
混合物共10g放入足量的稀硫酸中充分反应, 过滤得9.5g固体,则此混合物中Cu2O的质量分数为________。
《拓展与思考》:小华也用氢氧化钠溶液与硫酸铜溶液反应,但得到的沉淀不呈蓝色,而是浅绿色的;他又将此浊液加热直至沸腾,观察不到有分解变黑的迹象。为什么?小华查找资料得知,该浅绿色沉淀物是溶解度极小的碱式硫酸铜,其化学式为Cu4(OH)6SO4,同时还生成硫酸钠;此浅绿色沉淀能与酸反应,形成蓝色溶液。则碱式硫酸铜中铜元素的化合
价为______,请帮小华写出生成浅绿色沉淀的有关反应的化学方程式:_________________。
小华想设计一个实验,证明该浅绿色沉淀中含有硫酸根, 于是将沉淀过滤、洗涤,把沉淀再溶解在足量的无色溶液A中,取所得溶液滴加无色溶液B,若有大量白色沉淀生成,则表示原浅绿色沉淀中有SO42-,试推测:(1)无色溶液A的化学式是 ,无色溶液B的化学式是 ;
(2)写出产生白色溶液的化学方程式 。
《假设》:②可能是氧化铜 《设计实验》:略 《推测结论》:②
《形成结论》:Cu(OH)2 △ CuO+ H2O 《查阅资料》 ⑴A ⑵9%
《拓展与思考》:+2, 6NaOH+4CuSO4=Cu4(OH)6SO4↓+3Na2SO4
⑴A是HNO3(或HCl) B是Ba(NO3)2(或BaCl2)
⑵CuSO4+Ba(NO3)2= Cu(NO3)2+BaSO4↓ 或 CuSO4+BaCl2=CuCl2+BaSO4↓
解析:假设:根据质量守恒定律可知,反应前后元素的种类不变,可以有三种情况,即氧化铜、铜、氧化亚铜,故答案为:氧化铜,铜(写化学式也可).
推测结论:根据质量守恒定律可以假设三种情况,然后再结合颜色的不同可以断定是氧化铜(氧化铜是黑色,其他是红色);故答案为:质量守恒定律,铜与氧化亚铜固体不是黑色(或氧化铜是黑色粉末)
验证结论:氧化铜可以和稀硫酸反应生成蓝色溶液,其他不会和稀硫酸反应.故答案为:取少量黑色粉末放入试管中,加入足量稀硫酸; 黑色粉末逐渐消失,溶液变成蓝色.

 16、氢氧化铜固体受热分解能得到两种产物,其中一种为固定.某学生小组为确定这种固体产物是什么,进行了如下探究活动.
16、氢氧化铜固体受热分解能得到两种产物,其中一种为固定.某学生小组为确定这种固体产物是什么,进行了如下探究活动. 氢氧化铜固体受热分解能得到两种氧化物,一种为固体,另一种是无色液体.某化学活动小组为确定这种固体产物是什么,进行了如下探究活动.
氢氧化铜固体受热分解能得到两种氧化物,一种为固体,另一种是无色液体.某化学活动小组为确定这种固体产物是什么,进行了如下探究活动.