题目内容
(2006?茂名)某飞行器用肼(N2H4)和过氧化氢(H2O2)作为燃料,它们混合时发生如下反应:2H2O2+N2H4═A+4H2O,则A的化学式为( )
分析:在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变分析解决.
解答:解:由反应的化学方程式2H2O2+N2H4═A+4H2O可知,反应前氢原子的个数,8,氧是4,氮原子是2,由于反应前后原子的种类和个数不变,所以A中只能含有2个氮原子,所以A是氮气
故选B.
故选B.
点评:学会根据质量守恒定律和化学方程式计算某种物质的化学式,一定要记住反应前后原子的种类、原子个数均不变.

练习册系列答案
相关题目
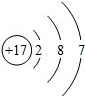 ,下列说法不正确的是( )
,下列说法不正确的是( )