题目内容
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g 全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。
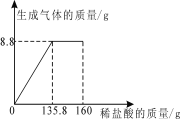
计算恰好完全反应时:
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数。(写出必要的计算过程,
结果保留到0.1%)
【答案】(1)8.8 (2)8.4%
【解析】
试题分析:(1)根据图像,可看出产生的二氧化碳的质量是8.8克
(2)根据化学方程式:Na2CO3+2HCl==2NaCl+H2O+CO2↑中Na2CO3、NaCl与CO2的质量关系,可求出Na2CO3的质量以及生成的氯化钠质量,进而求出所得到的溶液中溶质的质量分数
解:设Na2CO3的质量为x,NaCl的质量为y
Na2CO3+2HCl==2NaCl+H2O+CO2↑
106 117 44
x y 8.8g
106:44=x:8.8g x=21.2g
117:44=y:8.8g y=23.4g
故所得溶液中溶质的质量=2.34g+(23g-21.2g)=25.2g
所得到的溶液的质量=23g+150g+135.8g-8.8g=300g
所得到的溶液中溶质的质量分数=25.2g/300g×100%=8.8%

【题目】下列归纳内容全部正确的组别是
A.解释说明 | B.化学与生活 |
①稀有气体作保护气——化学性质稳定 ②O2、CO2化学性质不同——分子构成不同 ③众人拾柴火焰高——可燃物越多,燃烧越旺 | ①蛋白质、油脂、糖类都能为人体提供能量 ②人体所需维生素量不多,但不能缺少 ③玻璃钢、铝合金都是金属材料 |
C.化学用语中数字的含义 | D.方程式表示所述内容 |
① H2O:一个水分子含有两个氢原子 ② ③S2- :硫元素的化合价为负二价 | ①酸雨形成CO2+H2O==H2CO3 ②治疗胃酸过多Al(OH)3+3HCl==AlCl3+3H2O ③铝制品耐腐的原因:4Al+3O2==2Al2O3 |
【题目】小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe![]() Fe2(SO4)3+6 H2O +3SO2↑
Fe2(SO4)3+6 H2O +3SO2↑
(2)SO2可使品红溶液的红色褪去。
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫。
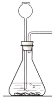
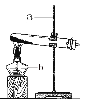
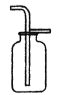
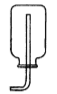
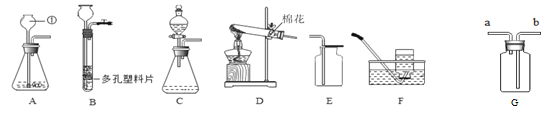
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验。
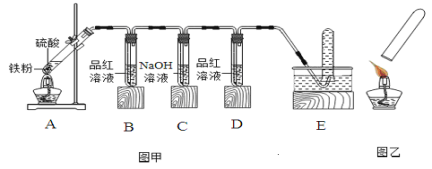
请帮助小明完成下表:
A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | |
实验三 | 25% | 不褪色 | _________ | 只有H2 | |
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫。
【交流反思】(1)写出实验三中铁与硫酸反应的化学方程式: 。
(2)实验一中C装置中反应的化学方程式:_____________________________。
【拓展延伸】在初中化学教材中也有反应物浓度不同,生成的产物不同的例子_______________________
_________________________________________________________________________________________