题目内容
【题目】实验室一般用氢氧化钠溶液吸收二氧化碳或二氧化硫。已知二氧化碳过量时,氢氧化钠全部转化成碳酸钠后,还会发生以下反应;Na2CO3+ H2O+CO2=2NaHCO3
(1)现在实验室用含氢氧化钠4.0g的溶液吸收二氧化碳,最多能产生NaHCO3多少克?(写出计算过程)_____________
(2)请在下图中画出产生碳酸氢钠的质量的变化曲线______________
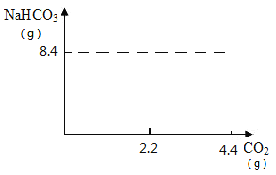
【答案】 8.4g 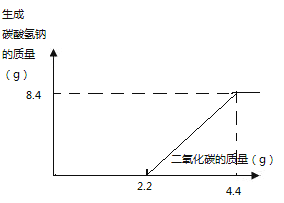
【解析】设实验室用含氢氧化钠4.0g的溶液吸收二氧化碳,最多能产生NaHCO3的质量为x
由方程式:2NaOH+CO2===Na2CO3+H2O, Na2CO3+ H2O+CO2=2NaHCO3,得关系式为
2NaOH ~ Na2CO3 ~ 2NaHCO3
80 168
4.0g x
80/4.0g=168/x x=8.4g
由方程式可知,开始通入二氧化碳生成碳酸钠,碳酸钠和二氧化碳再反应生成碳酸氢钠,所以图像为: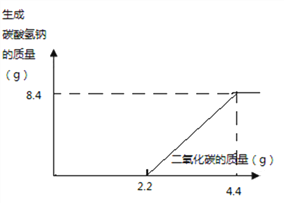

练习册系列答案
相关题目