题目内容
【题目】20℃时,取18gKNO3和18gNaCl分别放入两只烧杯中,各加入50mL水(水的密度为1g/mL),充分溶解,现象如图甲所示;升温到50℃时,现象如图乙所示,KNO3和NaCl的溶解度曲线如图丙,请回答下列问题: 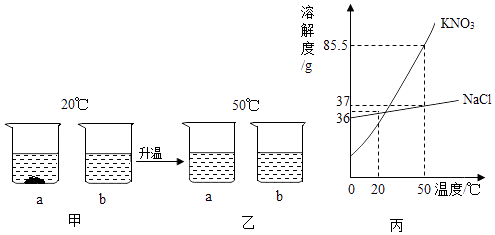
(1)a烧杯中加入的物质是(填化学式)
(2)甲图中,a烧杯溶液中溶质的质量分数(“>”、“<”或“=”)b烧杯溶液中溶质的质量分数.
(3)要使乙图中的NaCl溶液恰好变成饱和溶液,需要加入gNaCl固体.
(4)除去NaCl固体中混有的少量KNO3 , 实验步骤,先加水溶解,再 , 然后过滤,洗涤、干燥.
【答案】
(1)KNO3
(2)<
(3)0.5
(4)蒸发浓缩
【解析】解:(1)20℃时,氯化钠的溶解度大于硝酸钾的溶解度,取18gKNO3和18gNaCl分别放入两只烧杯中,各加入50ml水(水的密度为1g/mL),充分溶解,a烧杯底部有固体剩余,所以a烧杯中加入的物质是:KNO3;(2)甲图中,溶剂质量相等,a烧杯中的溶质质量小于b烧杯中的溶质质量,所以a烧杯溶液中溶质的质量分数<b烧杯溶液中溶质的质量分数;(3)50℃时,氯化钠的溶解度是37g,所以要使乙图中的NaCl溶液恰好变成饱和溶液,需要加入0.5gNaCl固体;(4)硝酸钾的溶解度受温度变化影响较大,所以除去NaCl固体中混有的少量KNO3,实验步骤,先加水溶解,再蒸发浓缩,然后过滤,洗涤、干燥.
所以答案是:(1)KNO3;(2)<;(3)0.5;(4)蒸发浓缩.
【考点精析】本题主要考查了结晶的原理、方法及其应用和饱和溶液和不饱和溶液相互转变的方法的相关知识点,需要掌握结晶的两种方法:蒸发溶剂,如NaCl(海水晒盐)和降低温度(冷却热的饱和溶液,如KNO3);饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂才能正确解答此题.

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案