题目内容
31、在实验课上,老师要同学们配制15%的氯化钠溶液50g.
(1)计算:配制15%的氯化钠溶液50g,需氯化钠的质量为
(2)甲同学按图所示步骤依次操作.

其错误的操作步骤有
E中玻璃棒的作用是
(3)乙同学在将称量好的氯化钠倒入烧杯中时,不小心有一部分氯化钠固体撒出,则其所配溶液溶质质量分数与15%相比
(1)计算:配制15%的氯化钠溶液50g,需氯化钠的质量为
7.5
g,水的体积为42.5
mL.(2)甲同学按图所示步骤依次操作.

其错误的操作步骤有
A
和B
(填字母序号);B中仪器名称为量筒
;E中玻璃棒的作用是
搅拌,加速溶解
.(3)乙同学在将称量好的氯化钠倒入烧杯中时,不小心有一部分氯化钠固体撒出,则其所配溶液溶质质量分数与15%相比
偏低
(答“偏低”、“偏高”、或“相等”)分析:(1)利用溶质质量=溶液质量×溶液中溶质质量分数,计算该溶液中氯化钠的质量,溶液质量与氯化钠质量差即为溶液中水的质量.
(2)根据药品的称量和液体的量取方法判断;
(3)根据溶质和溶液的质量关系判断.
(2)根据药品的称量和液体的量取方法判断;
(3)根据溶质和溶液的质量关系判断.
解答:解:
(1)50g 15%的氯化钠溶液中氯化钠的质量=50g×15%=7.5g,该溶液中溶剂水的质量=50g-7.5g=42.5g;
(2)错误的操作步骤有 A,没有按照左物右码的规定称量药品,B没有平视凹液面的最低处;B中仪器名称为量筒;E中玻璃棒的作用是搅拌,加速溶解.
(3)配制溶液过程中,溶质损失,溶液的溶质质量分数会减小.
故答案为:(1)7.5;42.5;
(2)A;B;量筒;搅拌,加速溶解;
(3)偏低
(1)50g 15%的氯化钠溶液中氯化钠的质量=50g×15%=7.5g,该溶液中溶剂水的质量=50g-7.5g=42.5g;
(2)错误的操作步骤有 A,没有按照左物右码的规定称量药品,B没有平视凹液面的最低处;B中仪器名称为量筒;E中玻璃棒的作用是搅拌,加速溶解.
(3)配制溶液过程中,溶质损失,溶液的溶质质量分数会减小.
故答案为:(1)7.5;42.5;
(2)A;B;量筒;搅拌,加速溶解;
(3)偏低
点评:配制溶液常见操作:固体溶质加水溶解,配制步骤计算、称量、溶解;注意正确的操作方法和正确的使用仪器.

练习册系列答案
相关题目
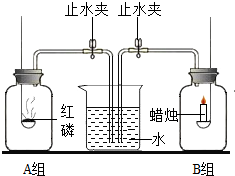 化学课上,陈老师说:“空气是人类和一切动植物的生命支柱,那么空气是由哪些物质组成的呢?请同学们设计不同测定空气中氧气含量的实验方案”.几分钟后,我们设计了如图所示A、B二组装置进行实验探究.
化学课上,陈老师说:“空气是人类和一切动植物的生命支柱,那么空气是由哪些物质组成的呢?请同学们设计不同测定空气中氧气含量的实验方案”.几分钟后,我们设计了如图所示A、B二组装置进行实验探究.