题目内容
【题目】生活离不开资源
(一)水的有关知识
下图是水厂利用水库中的水生产自来水的主要流程:请回答下列问题:
(1)高铁酸钠(Na2FeO4)是被科学家们公认为绿色消毒剂。其中铁元素的化合价为。
(2)日常生活中将上面清水池中的水煮沸,可以达到杀菌和的效果。
(3)(二)研究二氧化碳的性质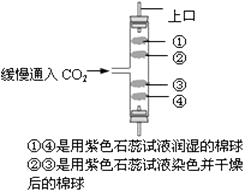
将二氧化碳缓慢通入竖直放置的玻璃管中,能观察到第(填序号)号棉球先变色,由此现象可知二氧化碳具有的物理性质。
(4)(三)探究燃烧的条件
通常情况下,燃烧需要三个条件,在下图所示的实验中,
能证明可燃物燃烧与温度有关的是。
(5)实验③和实验④证明燃烧和有关。
(6)(四)探究一氧化碳的性质和用途
学校化学兴趣小组的同学对一份固体样品进行了探究。通过实验已确定该样品由氧化铜和铜粉混合而成。他们称取了20g固体样品,用图1所示的装置继续实验,至反应完全测定的部分数据如图2所示。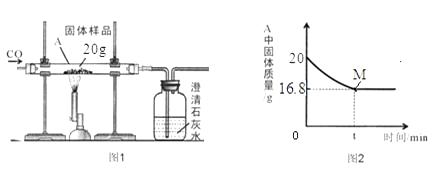
据图解决有关问题:
写出图1中硬质玻璃管中发生的化学方程式;
广口瓶中的现象是;图1实验中存在的明显缺陷是。
(7)图2中M点表示反应(填“进行中”或“结束”),图2 中16.8克物质是(填物质名称)
(8)原混合物中氧化铜的质量是克。
(9)假如产生的二氧化碳全部被澄清的石灰水吸收,产生的沉淀是多少克?(写出计算过程)
【答案】
(1)+6
(2)软化硬水
(3)④,密度比空气大
(4)②④
(5)O2
(6)CO+CuO ![]() Cu+CO2 ,石灰水变浑浊,没有尾气处理装置
Cu+CO2 ,石灰水变浑浊,没有尾气处理装置
(7)结束,铜
(8)16
(9)解:设产生的CO2质量为x,生成CaCO3质量为y
CO+ | CuO | CO2; | CO2+Ca(OH)2= | CaCO3↓+H2O |
80 | 44 | 44 | 100 | |
16g | x | 8.8g | y |
![]()
x=8.8g;y=20g
答:产生的沉淀是20g。
【解析】 (1)化合物中元素的化合价的代数和为零,设铁元素的化合价为x,则x+(+1)×2+(-2)×4=0得X=+6;
(2)煮沸可以将硬水中的钙镁化合物转化成沉淀而降低水的硬度将硬水软化;
(3) 二氧化碳的密度比空气大,能与水反应生成碳酸,使紫色石蕊变红;
(4)②冷水中和氧气接触的白磷不燃烧,④热水中和氧气接触的白磷燃烧,说明燃物燃烧与温度有关;
(5)实验③没有氧气,白磷不燃烧,和实验④接触氧气,白磷燃烧,证明燃烧需要可燃物与氧气充分接触;
(6)一氧化碳和氧化铜在加热条件下反应生成铜和二氧化碳,CO + CuO ![]() Cu +CO2二氧化碳使澄清石灰水变浑浊 ; 没有尾气处理装置,会导致一氧化碳排放到空气中,污染空气;
Cu +CO2二氧化碳使澄清石灰水变浑浊 ; 没有尾气处理装置,会导致一氧化碳排放到空气中,污染空气;
(7)M点物质的质量不再变化,表示反应结束;16.8克物质是反应后铜的质量;
(8)反应中物质减少的质量即为氧化铜中氧元素的质量,所以原混合物中氧化铜的质量是(20g-16.8g)÷(16÷80×100%)=16g;
(9)设产生的CO2质量为x,生成CaCO3质量为y,
CO+CuO ![]() Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O
Cu+CO2;CO2+Ca(OH)2=CaCO3↓+H2O
80 44 44 100
16g x 8.8g y
![]() =
=![]() ;
;![]() =
=![]()
x=8.8g;y=20g
答:产生的沉淀是20g。
所以答案是:(1)+6;(2)软化硬水;(3)④;密度比空气大;(4)②④;(5)O2;(6)CO+CuO ![]() Cu+CO2 ;石灰水变浑浊;没有尾气处理装置;(7)结束;铜;(8)16;(9)20.
Cu+CO2 ;石灰水变浑浊;没有尾气处理装置;(7)结束;铜;(8)16;(9)20.
【考点精析】关于本题考查的硬水与软水和根据化学反应方程式的计算,需要了解硬水和软水的鉴别方法:用肥皂水,有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水;各物质间质量比=系数×相对分子质量之比才能得出正确答案.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案