题目内容
【题目】向装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量.有关量的变化情况如图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化).其中肯定不正确的是( )
A.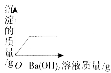
B.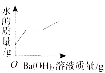
C.
D.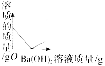
【答案】B
【解析】Ba(OH)2溶液与稀硫酸反应的化学方程式为:H2SO4+Ba(OH)2=BaSO4↓+2H2O.当烧杯中硫酸反应完时沉淀的质量不再增加,故A对;随着Ba(OH)2溶液的不断加入,烧杯中的水量不断增加,故B错;烧杯中的pH由小于7逐渐变为等于7,当硫酸反应完时,pH大于7,故C对;由于Ba(OH)2溶液与稀硫酸反应生成的BaSO4是一种沉淀,故在硫酸没有反应完之前,烧杯中溶质的质量不断减小,恰好完全反应时,烧杯中的溶质的质量为0,当硫酸反应完时,随着Ba(OH)2溶液的不断加入烧杯中的溶质又不断增加,故D对.

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目