题目内容
课外小组同学在实验室进行一氧化碳还原氧化铁的实验。
【查阅资料】
Ⅰ.常温下,甲酸(HCOOH)是无色易挥发的液体,在浓硫酸作用下易分解。甲酸分解的化学方程式为:HCOOH  CO↑+ H2O,浓硫酸在反应中起 作用。
CO↑+ H2O,浓硫酸在反应中起 作用。
Ⅱ.铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【实验设计及操作】
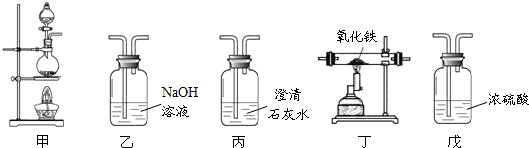
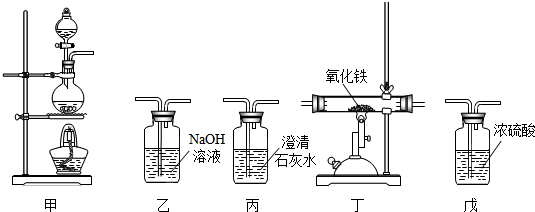
(1)利用下列装置完成用纯净、干燥的一氧化碳还原氧化铁实验,并检验气态产物。
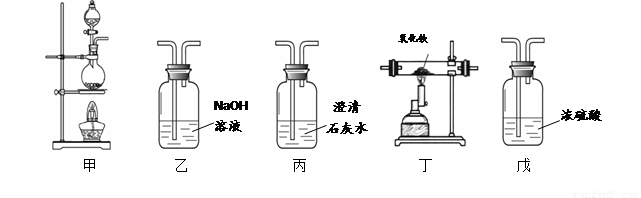
① 若各步均反应完全,装置的连接顺序为甲→ → → → →尾气处理(填序号)。
② 实验时先点燃甲中的酒精灯,一段时间后再点燃丁中的酒精喷灯,目的是 ;装置乙的作用是 。
③ 装置丁中观察到的现象是 ,反应的化学方程式是 。
(2)为检验氧化铁是否反应完全,同学们设计如下实验方案:从装置丁中取出少量反应后的固体粉末于试管中,加入足量稀盐酸,若观察到有大量气泡产生且溶液变为浅绿色而非黄色,则说明氧化铁已完全反应。上述判断是否正确,理由是 。
【查阅资料】催化(剂)
【实验设计及操作】
(1)①乙→戊→丁→丙 (1分,有错不得分)
②产生CO气体,排尽装置内的空气,防止加热爆炸 除去CO中易挥发的甲酸气体
③红色粉末变成黑色 Fe2O3 + 3CO 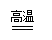 2Fe + 3CO2
2Fe + 3CO2
(2)不正确(1分), 未反应的氧化铁与盐酸反应生成氯化铁溶液,氯化铁溶液与生成的铁反应生成氯化亚铁,溶液也可变为浅绿色。(1分)
【解析】【查阅资料】甲酸在浓硫酸作用下易分解,所以浓硫酸起催化作用。
(1)①先将气体通过氢氧化钠把挥发出的甲酸除掉,在经过浓硫酸干燥一下,就可以得到纯净的一氧化碳了,经过氧化铁,在经过石灰水来检验气体产物,故连接顺序为乙→戊→丁→丙,
②因为刚开始管内有空气,一氧化碳中混有空气,容易发生爆炸,所以要先点燃甲中的酒精灯,一段时间后再点燃丁中的酒精喷灯产生CO气体,排尽装置内的空气。装置乙的作用是除去CO中易挥发的甲酸气体。
③一氧化碳还原氧化铁的现象为红色粉末变成黑色方程式为Fe2O3
+ 3CO =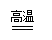 ==
2Fe + 3CO2
==
2Fe + 3CO2
(2)因为氯化铁也能和铁反应,生成氯化亚铁,故不正确。

 孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.
孔雀石[碱式碳酸铜,主要成分是Cu2(OH)2CO3]具有色彩浓淡的条状花纹(如图),是矿物中最吸引人的装饰材料之一,也是人类最早冶炼铜的原料.冶炼铜的反应原理为:Cu(OH)2CO3
| ||
2CuO+C
| ||
某校课外小组同学在实验室验证上述反应.
(1)加热分解碱式碳酸铜,生成氧化铜.装置如下图所示.
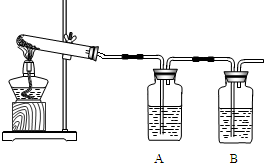
①瓶A中盛有的试剂是
②瓶B中盛有的试剂是澄清石灰水,用来
③反应结束,熄灭酒精灯前,应
(2)木炭和氧化铜反应,生成铜.
将木炭粉末和氧化铜粉末混合均匀,放进试管,加热充分反应.将试管中的粉末倒出,有铜生成,还有少量黑色粉末剩余.该小组同学设计方案验证黑色粉末的成分.
查阅资料:部分内容如下:木炭和氧化铜都是黑色粉末.氧化铜与稀硫酸反应生成硫酸铜,木炭与稀硫酸不反应.
| 操作和药品 | 现象 | 分析和结论 | |
| 方案Ⅰ | 取少量剩余黑色粉末,充分灼烧 | ①______________ ________________ |
原剩余黑色粉末是 氧化铜 |
| 方案Ⅱ | ②_______________ __________________ |
③_____________ _________________ |
原剩余黑色粉末是 氧化铜 |
(3)某同学探究在实际反应中,木炭和氧化铜反应生成铜时反应物的最佳质量比.设计方案如下:
| 配方1 | 配方2 | 配方3 | 配方4 | |
| 木炭质量(g) | 0.4 | 0.5 | 0.6 | 0.7 |
| 氧化铜质量(g) | 8 | 8 | 8 | 8 |
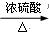 CO↑+ H2O。
CO↑+ H2O。
 CO↑+ H2O。
CO↑+ H2O。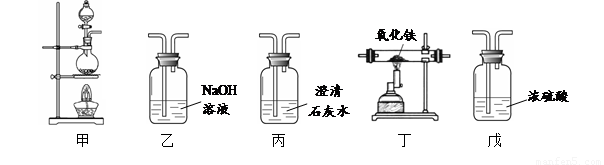
 CO↑+H2O.
CO↑+H2O.