题目内容
 下表为KCl、NaCl和KNO3在不同温度时的溶解度,如图为它们的溶解度曲线.
下表为KCl、NaCl和KNO3在不同温度时的溶解度,如图为它们的溶解度曲线.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 42.6 | 45.5 | 51.1 |
| NaCl | 36.0 | 36.3 | 37.0 | 37.3 | 38.4 | |
| KNO3 | 31.6 | 45.8 | 85.5 | 110.0 | 169.0 | |
(2)如图中表示KNO3溶解度曲线的是
(3)30℃时,向45.8g KNO3固体中加入100g水,充分溶解后升温至40℃,该溶液中溶质的质量分数
(4)要将丙的不饱和溶液转化为饱和溶液适宜的方法是
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数
专题:溶液、浊液与溶解度
分析:(1)根据表中的信息可确定 30℃时KCl的溶解度;
(2)对比溶解度随温度变化明显与不明显;硝酸钾的溶解度受温度影响变化较大;
(3)根据表中的信息可确定 30℃时KNO3的溶解度为45.8g解答;
(4)根据丙的溶解度随温度变化不大解答.
(2)对比溶解度随温度变化明显与不明显;硝酸钾的溶解度受温度影响变化较大;
(3)根据表中的信息可确定 30℃时KNO3的溶解度为45.8g解答;
(4)根据丙的溶解度随温度变化不大解答.
解答:解:
(1)根据表中的信息可确定 30℃时KCl的溶解度为37.0g;故答案为36.0g
(2)根据表中的信息可确定硝酸钾的溶解度随温度变化明显,而氯化钾的溶解度随温度变化很不明显,故答案为:甲;
(3)30℃时KNO3的溶解度为45.8g,100g水中最多溶解45.8g,向45.8g KNO3固体中加入100g水,恰好完全溶解,由于硝酸钾的溶解度随温度的升高而增大,升温至40℃,变为不饱和溶液,溶质质量和溶剂质量不变,该溶液中溶质的质量分数不变;
(4)丙的溶解度随温度变化不大,将丙的不饱和溶液转化为饱和溶液适宜的方法是蒸发结晶.
答案:
(1)36.0g
(2)甲
(3)不变
(4)蒸发结晶
(1)根据表中的信息可确定 30℃时KCl的溶解度为37.0g;故答案为36.0g
(2)根据表中的信息可确定硝酸钾的溶解度随温度变化明显,而氯化钾的溶解度随温度变化很不明显,故答案为:甲;
(3)30℃时KNO3的溶解度为45.8g,100g水中最多溶解45.8g,向45.8g KNO3固体中加入100g水,恰好完全溶解,由于硝酸钾的溶解度随温度的升高而增大,升温至40℃,变为不饱和溶液,溶质质量和溶剂质量不变,该溶液中溶质的质量分数不变;
(4)丙的溶解度随温度变化不大,将丙的不饱和溶液转化为饱和溶液适宜的方法是蒸发结晶.
答案:
(1)36.0g
(2)甲
(3)不变
(4)蒸发结晶
点评:此题是溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也复习了有关混合物分离的一些常识性的基础知识.

练习册系列答案
相关题目
200多年前,法国化学家拉瓦锡用定量方法研究空气成分,其中一项实验是加热红色氧化汞粉末得到汞和氧气,该反应示意图如下:
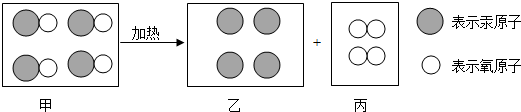
下列说法正确的是( )

下列说法正确的是( )
| A、该反应是氧化反应 |
| B、图中甲、乙、丙三种物质均是由分子构成的 |
| C、保持汞的化学性质的最小粒子是汞原子 |
| D、该反应前后分子种类、原子种类均没有改变 |
从人体呼出的气体可以使( )
①带火星的木条复燃 ②澄清的石灰水变浑浊 ③燃着的木条燃烧更旺.
①带火星的木条复燃 ②澄清的石灰水变浑浊 ③燃着的木条燃烧更旺.
| A、①③ | B、② | C、①② | D、③ |
下列有关氧气的叙述不正确的是( )
| A、氧气能使带火星的木条复燃 |
| B、硫在氧气中燃烧时,发出微弱的淡蓝色火焰,生成刺激性气味的气体 |
| C、红磷在空气中燃烧产生大量白烟,生成白色固体 |
| D、物质与氧气发生的反应都是氧化反应 |
下列主要发生物理变化的是( )
A、 铜锭拉成铜丝 |
B、 铁生锈 |
C、 加热金属铜 |
D、 蜡烛燃烧 |
 测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.
测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少容积,做上记号.用弹簧夹夹紧乳胶管.点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧.