题目内容
【题目】化学是从微观的角度研究物质的组成、结构及其变化的学科。构成物质的粒子之间关系如图所示。 回答下列问题:
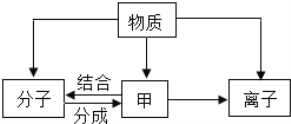
(1)甲是__________ 。
(2)在水、汞和氯化钠三种物质中,由离子构成的物质是 ____________ 。保持水的化学性质的最小粒子是_____________ 。
(3)从微观来看,化学反应的实质是 _______________________________________。
【答案】 原子 NaCl(或氯化钠) 水分子(或H2O分子) 分子分成原子,再重新组合成新物质的分子
【解析】(1)构成物质的粒子有分子、原子和离子,其中分子是由原子构成的,原子得失电子形成离子;(2)水是由水分子构成的,汞是由汞原子构成的,氯化钠是由钠离子和氯离子构成的;(3)化学变化是生成新分子的变化,其实质是分子分解成原子,原子重新组合形成新的分子。

练习册系列答案
相关题目