题目内容
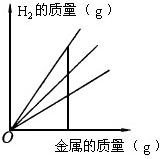
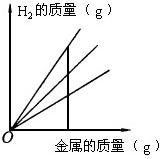 用铁、镁、铝分别与足量的盐酸反应制取氢气,下图是产生氢气的质量与所用金属质量的关系图.如果a代表铁,b代表镁,c代表铝,这三条图线从上到下的顺序是( )
用铁、镁、铝分别与足量的盐酸反应制取氢气,下图是产生氢气的质量与所用金属质量的关系图.如果a代表铁,b代表镁,c代表铝,这三条图线从上到下的顺序是( )| A、a,b,c | B、b,c,a | C、c,a,b | D、c,b,a |
分析:根据等质量的三种金属与酸完全反应放出氢气质量的大小,判断关系图中三条线与金属的对应关系.
解答:解:假设等质量的三种金属的质量为m,与酸完全反应放出氢气质量为:
铝完全反应放出氢气质量=
×m=
镁完全反应放出氢气质量=
×m=
铁完全反应放出氢气质量=
×m=
则关系图中三条线从上到下的顺序为:c,b,a.
故选D
铝完全反应放出氢气质量=
| 3 |
| 27 |
| m |
| 9 |
镁完全反应放出氢气质量=
| 2 |
| 24 |
| m |
| 12 |
铁完全反应放出氢气质量=
| 2 |
| 56 |
| m |
| 28 |
则关系图中三条线从上到下的顺序为:c,b,a.
故选D
点评:等质量的镁、铝、锌、铁与酸完全反应放出氢气的质量由大到小的关系为:铝>镁>铁>锌.

练习册系列答案
相关题目
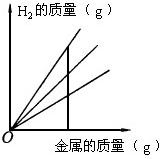 用铁、镁、铝分别与足量的盐酸反应制取氢气,下图是产生氢气的质量与所用金属质量的关系图.如果a代表铁,b代表锌,c代表铝,这三条图线从上到下的顺序是
用铁、镁、铝分别与足量的盐酸反应制取氢气,下图是产生氢气的质量与所用金属质量的关系图.如果a代表铁,b代表锌,c代表铝,这三条图线从上到下的顺序是