题目内容
(2009?崇明县二模)根据下列实验装置图,回答下列问题:
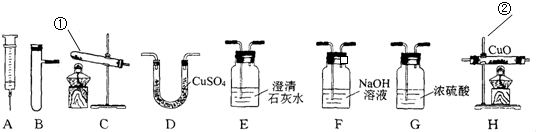
(1)写出图中标有①和②的仪器名称:①
(2)甲同学用氯酸钾与二氧化锰混合加热的方法制取氧气,他选用了C装置,向C装置内加药品前,应该进行的操作是
(3)在用过氧化氢(H2O2)溶液与二氧化锰混合制取氧气时,在选用发生装置时,乙同学选用了A与B,丙同学选用了B,请比较乙同学选用的发生装置的优点是
(4)用大理石与稀盐酸反应制取二氧化碳的化学方程式是
(5)如果用一氧化碳还原H装置中的CuO,若要生成0.1摩尔的铜,则需要消耗氧化铜的质量为多少克?(写出计算过程)
(6)某无色气体可能由H2、CO或CO2中的一种或几种组成,若将该气体先通过H装置,再通入E装置,可看到H中黑色粉末变为光亮的红色,E中澄清石灰水变浑浊,则该气体的组成情况可能是

(1)写出图中标有①和②的仪器名称:①
试管
试管
②铁架台
铁架台
(2)甲同学用氯酸钾与二氧化锰混合加热的方法制取氧气,他选用了C装置,向C装置内加药品前,应该进行的操作是
检查装置的气密性
检查装置的气密性
,反应中二氧化锰的作用是催化作用
催化作用
,该反应的化学方程式是2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
,属于基本反应类型中的
| ||
| △ |
分解
分解
反应.(3)在用过氧化氢(H2O2)溶液与二氧化锰混合制取氧气时,在选用发生装置时,乙同学选用了A与B,丙同学选用了B,请比较乙同学选用的发生装置的优点是
可随时添加液体药品
可随时添加液体药品
(写一个即可).实验结束后,乙同学用带火星的木条伸入集气瓶内,木条没有复燃;请你帮助乙同学分析导致这种现象的原因装置漏气没有收集到氧气
装置漏气没有收集到氧气
(写一个即可).(4)用大理石与稀盐酸反应制取二氧化碳的化学方程式是
CaCO3+2HCl=CaCl2+H2O+CO2↑.
CaCO3+2HCl=CaCl2+H2O+CO2↑.
,检验二氧化碳中混有水蒸气,最好选用D
D
装置(用序号表示),该反应的化学方程式是CuSO4+5H2O═CuSO4?5H2O
CuSO4+5H2O═CuSO4?5H2O
.(5)如果用一氧化碳还原H装置中的CuO,若要生成0.1摩尔的铜,则需要消耗氧化铜的质量为多少克?(写出计算过程)
(6)某无色气体可能由H2、CO或CO2中的一种或几种组成,若将该气体先通过H装置,再通入E装置,可看到H中黑色粉末变为光亮的红色,E中澄清石灰水变浑浊,则该气体的组成情况可能是
CO或CO和CO2
CO或CO和CO2
.分析:(1)根据常用仪器的名称和用途判断;
(2)制取气体加入药品前应检查装置的气密性,二氧化锰在氯酸钾反应中起催化作用,再根据氯酸钾反应原理书写方程式,依据反应特点判断反应类型;
(3)对比两套装置,分析乙同学选用的发生装置的优点,带火星的木条伸入集气瓶内,木条没有复燃,可能原因有装置漏气没有收集到氧气(或反应物的量不够或收集的氧气不纯);
(4)根据反应原理书写方程式,检验二氧化碳中混有水蒸气,最好选用硫酸铜,遇水生成五水合硫酸铜,由白色变蓝色,再依据反应原理书写方程式;
(5)根据一氧化碳还原氧化铜的化学方程式,计算参加反应的氧化铜的质量;
(6)结合题意,并根据氢气和一氧化碳还原氧化铜的生成物及二氧化碳可使澄清的石灰水变浑浊解答.
(2)制取气体加入药品前应检查装置的气密性,二氧化锰在氯酸钾反应中起催化作用,再根据氯酸钾反应原理书写方程式,依据反应特点判断反应类型;
(3)对比两套装置,分析乙同学选用的发生装置的优点,带火星的木条伸入集气瓶内,木条没有复燃,可能原因有装置漏气没有收集到氧气(或反应物的量不够或收集的氧气不纯);
(4)根据反应原理书写方程式,检验二氧化碳中混有水蒸气,最好选用硫酸铜,遇水生成五水合硫酸铜,由白色变蓝色,再依据反应原理书写方程式;
(5)根据一氧化碳还原氧化铜的化学方程式,计算参加反应的氧化铜的质量;
(6)结合题意,并根据氢气和一氧化碳还原氧化铜的生成物及二氧化碳可使澄清的石灰水变浑浊解答.
解答:解:(1)根据常用仪器的名称和用途判断可知仪器分别是:试管和铁架台;
故答案为:试管;铁架台;
(2)制取气体加入药品前应检查装置的气密性,二氧化锰在氯酸钾反应中起催化作用,氯酸钾在加热的条件下,二氧化锰作催化剂生成氯化钾和氧气,方程式是2KClO3
2KCl+3O2↑,该反应由一种物质生成两种物质,符合分解反应特点,属于分解反应;
故答案为:检查装置的气密性;催化作用;2KClO3
2KCl+3O2↑;分解反应;
(3)对比两套装置,可知乙同学选用的发生装置具有可随时添加液体药品和控制反应速率的特点,将带火星的木条伸入集气瓶内,木条没有复燃,可能原因有装置漏气没有收集到氧气(或反应物的量不够或收集的氧气不纯);
故答案为:可随时添加液体药品;装置漏气没有收集到氧气;(合理答案均可)
(4)大理石的主要成分碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,检验二氧化碳中混有水蒸气,最好选用硫酸铜,其遇水生成五水合硫酸铜,由白色变蓝色,可根据颜色改变判断生成水蒸气,方程式是CuSO4+5H2O═CuSO4?5H2O;
(5)0.1摩尔的铜的质量是:0.1×64=6.4g
设需要氧化铜的质量为x
CuO+CO
Cu+CO2
80 64
x 6.4g
=
x=8g
答:需要氧化铜8g.
(6)H中黑色粉末变为光亮的红色,说明气体中一定含有还原性气体,E中澄清石灰水变浑浊说明从H中出来的气体一定含有二氧化碳,一氧化碳可还原氧化铜生成红色的铜和二氧化碳,结合题意,可知气体可能是一氧化碳,也可能是一氧化碳和二氧化碳的混合物,H中无水珠,故无氢气;
故答案为:CO或CO和CO2
故答案为:试管;铁架台;
(2)制取气体加入药品前应检查装置的气密性,二氧化锰在氯酸钾反应中起催化作用,氯酸钾在加热的条件下,二氧化锰作催化剂生成氯化钾和氧气,方程式是2KClO3
| ||
| △ |
故答案为:检查装置的气密性;催化作用;2KClO3
| ||
| △ |
(3)对比两套装置,可知乙同学选用的发生装置具有可随时添加液体药品和控制反应速率的特点,将带火星的木条伸入集气瓶内,木条没有复燃,可能原因有装置漏气没有收集到氧气(或反应物的量不够或收集的氧气不纯);
故答案为:可随时添加液体药品;装置漏气没有收集到氧气;(合理答案均可)
(4)大理石的主要成分碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑,检验二氧化碳中混有水蒸气,最好选用硫酸铜,其遇水生成五水合硫酸铜,由白色变蓝色,可根据颜色改变判断生成水蒸气,方程式是CuSO4+5H2O═CuSO4?5H2O;
(5)0.1摩尔的铜的质量是:0.1×64=6.4g
设需要氧化铜的质量为x
CuO+CO
| ||
80 64
x 6.4g
| 80 |
| x |
| 64 |
| 6.4g |
x=8g
答:需要氧化铜8g.
(6)H中黑色粉末变为光亮的红色,说明气体中一定含有还原性气体,E中澄清石灰水变浑浊说明从H中出来的气体一定含有二氧化碳,一氧化碳可还原氧化铜生成红色的铜和二氧化碳,结合题意,可知气体可能是一氧化碳,也可能是一氧化碳和二氧化碳的混合物,H中无水珠,故无氢气;
故答案为:CO或CO和CO2
点评:本题考查了实验室制取气体装置的选取、反应原理、仪器,化学方程式的计算等知识,考查知识全面且比较综合,难度稍大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目