题目内容
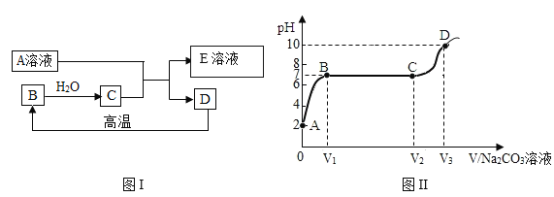
【题目】图示中A-E是初中化学常见的物质。C为单质,ABDE为四种不同类别化合物,其中E为大理石的主要成分。图中“一”表示相连的两种物质之间可以发生反应,“→”表示物质间存在着相应的转化关系(部分反应物、生成物及反应条件已略去)。
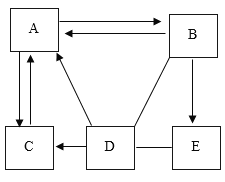
(1)物质E的化学式为_____。
(2)写出B物质的一种用途_____。
(3)反应A→C的基本反应类型为_____。
(4)B→A的化学方程式为_____。
【答案】CaCO3 改良酸性土壤 分解反应 ![]()
【解析】
根据E为大理石主要组分,可知E为碳酸钙,D可以与盐反应,又可以生成单质C,同时D与B可以反应,而ABD则不再属于盐,应从酸、碱和氧化物中选择,符合D性质则为酸,常见酸为盐酸,所以D为盐酸,盐酸可以生成的单质,则是其与金属反应生成氢气,所以C为氢气,E为碳酸钙,B可以生成E,说明E含有钙元素,符合碱的性质,所以B为氢氧化钙,A可以生成C氢气,而C氢气又可以生成A,符合此性质A为水,同时A水与B氢氧化钙可以相互转化制备,因此可以得出A为水,B为氢氧化钙,C为氢气,D为盐酸,E为碳酸钙。
(1)根据题目信息可知,E为碳酸钙,化学式为CaCO3;
故答案为:CaCO3。
(2)氢氧化钙属于碱,可以改良酸性土壤,利于作物的生长;
故答案为:改良酸性土壤。
(3)水在通电条件下反应生成氢气和氧气,一种反应物生成两种生成物,符合分解反应的特点,所以属于分解反应;
故答案为:分解反应。
(4)B为氢氧化钙,A为水,氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,此反应的化学方程式为![]() ;
;
故答案为:![]() 。
。

【题目】下表列出了固体物质A在不同温度时的溶解度
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
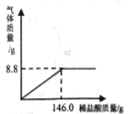
(1)80℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解后形成溶液的质量为_____g,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____(填最简整数比)。
(2)通过对上表数据的分析,物质A的溶解度曲线应是图中的_____(填“甲”或“乙”)。
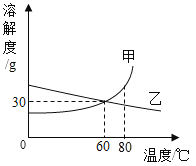
(3)80℃时,配制一定量甲物质的溶液,将其降温到60℃,是否有固体析出?_____(填“有”、“没有”或“不确定”)。