题目内容
【题目】在等质量的锌、铁中分别滴加等质量分数的稀硫酸至过量,产生氢气的质量随硫酸的质量变化曲线如图。
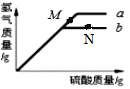
下列说法正确的是
A. b曲线表示锌与稀硫酸反应产生氢气的过程
B. M点对应溶液的溶质是硫酸和硫酸亚铁
C. 充分反应后,溶液的质量都增大
D. N点对应溶液中的溶质只有一种
【答案】AC
【解析】A、由方程式Fe+H2SO4=FeSO4+H2↑;
56 2
Zn+H2SO4=ZnSO4+H2↑
65 2
可知等质量的铁放出的气体大于锌放出的气体,所以b曲线表示锌与稀硫酸反应产生氢气的过程,故正确;
B、a曲线表示铁与稀硫酸反应产生氢气的过程,M点表示铁过量,硫酸不足,对应溶液的溶质只有硫酸亚铁,故错误;
C、由方程式Fe+H2SO4=FeSO4+H2↑;
56 2
Zn+H2SO4=ZnSO4+H2↑
65 2
充分反应后,溶液的质量都增大,故正确;
D、b曲线表示锌与稀硫酸反应产生氢气的过程,N点表示稀硫酸过量,对应溶液中的溶质是硫酸和硫酸锌,故错误。

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目