题目内容
经测定,某含有碳、氧两种元素组成的混合气体中,碳元素的质量分数为30%,则混合气体中一定含有的是
- A.氧气
- B.一氧化碳
- C.二氧化碳
- D.二氧化碳和一氧化碳
B
分析:先计算出含有C、O两种元素的常见气体中C元素的质量分数,然后根据已知条件“C元素的质量分数为30%”进行推断.
解答:若气体为一氧化碳气体;那么CO中C元素的质量分数为: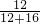 ×100%≈43%,也就是说,如果全部是CO的话,C元素的质量分数应该为43%;
×100%≈43%,也就是说,如果全部是CO的话,C元素的质量分数应该为43%;
若气体为二氧化碳气体;CO2中C元素的质量分数为: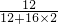 ×100%≈27%,即是说,如果全部是CO2的话,则C元素的质量分数应该为27%;
×100%≈27%,即是说,如果全部是CO2的话,则C元素的质量分数应该为27%;
如果是CO2与CO混合,那么C元素的质量分数必然介于43%与27%之间,这包含了30%,也就是说这种情况是可能的;
以此类推,CO与O2混合也是可能的,甚至三种气体同时存在也是有可能的.
但是如果是CO2与O2混合,则C元素只能在27%与0%之间,因此是不可能的.
综合上述所有可能情况,必然有CO.
故选B.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.
分析:先计算出含有C、O两种元素的常见气体中C元素的质量分数,然后根据已知条件“C元素的质量分数为30%”进行推断.
解答:若气体为一氧化碳气体;那么CO中C元素的质量分数为:
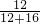 ×100%≈43%,也就是说,如果全部是CO的话,C元素的质量分数应该为43%;
×100%≈43%,也就是说,如果全部是CO的话,C元素的质量分数应该为43%;若气体为二氧化碳气体;CO2中C元素的质量分数为:
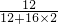 ×100%≈27%,即是说,如果全部是CO2的话,则C元素的质量分数应该为27%;
×100%≈27%,即是说,如果全部是CO2的话,则C元素的质量分数应该为27%;如果是CO2与CO混合,那么C元素的质量分数必然介于43%与27%之间,这包含了30%,也就是说这种情况是可能的;
以此类推,CO与O2混合也是可能的,甚至三种气体同时存在也是有可能的.
但是如果是CO2与O2混合,则C元素只能在27%与0%之间,因此是不可能的.
综合上述所有可能情况,必然有CO.
故选B.
点评:本题主要考查学生运用化学式和元素的质量分数公式进行计算的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目