题目内容
实验室用16g高锰酸钾放在试管中加热,反应后称得剩余固体物质的质量为14.4g.则剩余物质是( )A.锰酸钾
B.二氧化锰和锰酸钾
C.高锰酸钾和锰酸钾
D.二氧化锰、锰酸钾和高锰酸钾
【答案】分析:根据质量守恒定律,写出该反应的化学方程式,可知减少的固体质量是生成氧气的质量,根据生成氧气的质量即可求出参加反应的高锰酸钾的质量,从而可以判断剩余固体中是否有未反应的高锰酸钾,加热高锰酸钾,剩余固体中一定含有二氧化锰和锰酸钾.
解答:解:根据质量守恒定律,当固体质量变为14.4g时,生成氧气的质量为:16g-14.4g=1.6g.
设生成1.6g氧气,反应的高锰酸钾的质量为x g
2KMnO4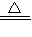 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
316 32
x 1.6g
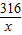 =
=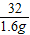
x=15.8g
故剩余的高锰酸钾的质量为16g-15.8g=0.2g.
由此可知剩余固体物质是:高锰酸钾、二氧化锰和锰酸钾;
故选D.
点评:本题主要考查学生对化学反应方程式的书写,以及运用质量守恒定律、方程式进行计算的能力.
解答:解:根据质量守恒定律,当固体质量变为14.4g时,生成氧气的质量为:16g-14.4g=1.6g.
设生成1.6g氧气,反应的高锰酸钾的质量为x g
2KMnO4
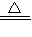 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑316 32
x 1.6g
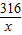 =
=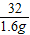
x=15.8g
故剩余的高锰酸钾的质量为16g-15.8g=0.2g.
由此可知剩余固体物质是:高锰酸钾、二氧化锰和锰酸钾;
故选D.
点评:本题主要考查学生对化学反应方程式的书写,以及运用质量守恒定律、方程式进行计算的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目