题目内容
【题目】金属材料与人类的生产和生活密切相关。请回答:
(1)铝通常被用于制作电线,这是利用了它的______性和______性
(2)工业上利用“铝热反应”焊接钢轨其原理是在高温下用铝将氧化铁中的铁置换出来。写出反应的化学方程式:______
(3)中国高铁制造处于世界先进水平,福建是全国第一个市市通高铁的省份。高铁建设需要大量的钢铁,高炉炼铁的主要原理是利用一氧化碳在高温下还原氧化铁,反应的化学方程式为______
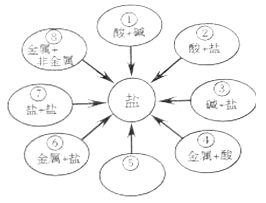
(4)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是______(填序号)
①将铝、银分别浸入到硫酸铜溶液中②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中④将铜分别浸入到硫酸铝、硝酸银溶液中
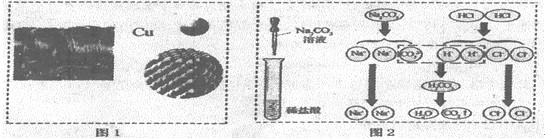
(5)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,得到滤渣和滤液。
①滤液中一定含有的溶质是______(填化学式);②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是______(填化学式)。
【答案】导电 延展 2Al+Fe2O3![]() 2Fe+Al2O3 3CO+Fe2O3
2Fe+Al2O3 3CO+Fe2O3![]() 2Fe+3CO2 ①④ MgCl2 Fe、Cu
2Fe+3CO2 ①④ MgCl2 Fe、Cu
【解析】
(1)铝通常被用于制作电线,这是利用了它的导电性和延展性
(2)工业上利用“铝热反应”焊接钢轨其原理是在高温下用铝将氧化铁中的铁置换出来。反应的化学方程式是:2Al+Fe2O3![]() 2Fe+Al2O3;
2Fe+Al2O3;
(3)高炉炼铁的主要原理是利用一氧化碳在高温下还原氧化铁,反应的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4))①将铝、银分别浸入到硫酸铜溶液中,由于铝能置换出溶液中的铜,银不能置换出溶液中的铜,所以,三种金属的活动性顺序是:铝>铜>银;
②将将银分别浸入到硫酸铝、硫酸铜溶液中,由于银不能置换出溶液中的锌、铜,不能比较铝、铜的活动性;
③将铜、银分别浸入到硫酸铝溶液中。由于铜、银都不能置换出溶液中的铝,不能比较铝、铜的活动性;
④将铜分别浸入到硫酸铝、硝酸银溶液中,由于铜不能置换出溶液中的铝,铜能置换出溶液中的银,所以,三种金属的活动性顺序是:铝>铜>银。
(5)在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,首先镁粉和氯化铜溶液反应,置换出单质铜,如果镁粉足量可以再继续和氯化亚铁反应置换出铁,所以:
①滤液中一定含有的溶质是MgCl2;
②向滤渣中滴加稀盐酸,有气泡产生,说明了有置换出的铁,则滤渣中一定含有的物质是:Fe、Cu。

【题目】从微观角度探析宏观的变化是化学学习的特点之一,请据表回答:
甲 | 乙 |
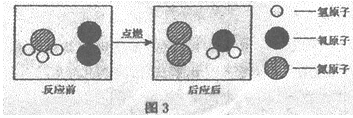
实验一:水沸腾实验二:水的分解 |
|
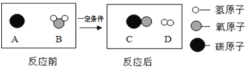
(1)乙中的微观过程对应甲中的实验______(选填“一”或“二”);
(2)请你将乙中的B图缺少的粒子补全______;
(3)在此变化中不发生改变的粒子是______。