题目内容
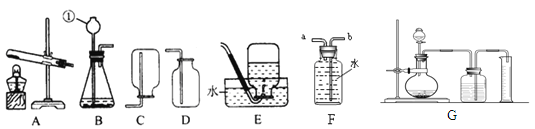
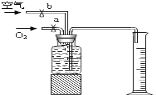
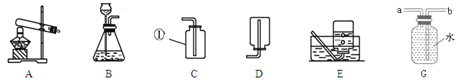
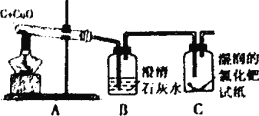
【题目】(8分)李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜(如下图),反应的化学方程式为:C+2CuO 高温 2Cu+CO2↑,他联想到单质碳的一些化学性质,认为在该实验中还可能会有CO产生。
查阅资料:CO气体能使湿润的黄色氯化钯试纸变蓝色。
实验验证:
(1)点燃A处酒精灯,数分钟后发现试管中的黑色固体物质变红,该红色物质是___________;
(2)装置B中发生的实验现象是__________________________,
该反应的化学方程式是___________________________;
(3)C装置中湿润的黄色氯化钯试纸变蓝色,说明有______气体生成,证明李洋同学是判断是正确的。
实验反思:
(4)李洋同学对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
②原因二:反应C+2CuO 高温 2Cu+CO2↑中的一种产物和反应物木炭又发生了新的化学反应,产生了CO;
③原因三:……
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理:
_____________________________ _____________。
(5)在设计装置时还要考虑环保因素,因此要在装置C处添加__ _________装置。
【答案】(1)铜 (2)澄清的石灰水变浑浊 ,Ca(OH)2+CO2==CaCO3↓+H2O;(3)CO
(4)C+CO2![]() 2CO (5)尾气处理装置
2CO (5)尾气处理装置
【解析】
试题分析:碳还原氧化铜生成的是铜和二氧化碳,现象是黑色的固体变成红色,生成了一种能使澄清石灰水变浑浊的气体:Ca(OH)2+CO2==CaCO3↓+H2O;根据资料:CO气体能使湿润的黄色氯化钯试纸变蓝色,现C装置中湿润的黄色氯化钯试纸变蓝色,说明产物中有一氧化碳;碳能还原二氧化碳生成一氧化碳,一氧化碳有毒,直接排放到空气中会污染空气,故要添加一个尾气处理装置,如把尾气点燃。