题目内容
【题目】铅蓄电池在生产、生活中使用广泛,其构造示意图如图所示,请回答下列问题:
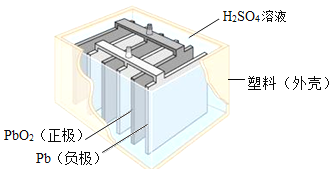
(1)铅蓄电池充电时是将电能转化为_________ 能。
(2)铅蓄电池放电过程中,发生反应的化学方程式为Pb+PbO2+2H2SO4 = 2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断_________(填“增大”、“减小”或“不变”)。
(3)从材料分类角度看,塑料是一种____________材料。(填“合成”或“复合”)
(4)废硫酸直接排放会污染环境,可以用熟石灰中和硫酸,发生反应的化学方程式是________。
【答案】化学 增大 合成 Ca(OH)2+H2SO4=CaSO4+2H2O
【解析】
(1)铅蓄电池也是化学电池,在充电时,消耗电能,得到化学能,故充电时将电能转化为化学能;
(2)硫酸被消耗,所以酸性减弱,pH不断增大;
(3)从材料分类角度看,塑料是一类有机合成材料。
(4)熟石灰为氢氧化钙,它与硫酸反应生成硫酸钙和水,反应的化学方程式为:![]() 。
。

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
【题目】氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。用它制备氢氧化镁的流程示意图如下:

部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
开始沉淀 | 1.9 | 4.2 | 9.1 |
完全沉淀 | 3.2 | 6.7 | 11.1 |
(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。