题目内容
(2013?顺义区二模)浓硫酸具有吸水性,可以做干燥剂,而稀硫酸不能.好奇心强的同学提出问题:浓硫酸的浓度降低到什么程度时就不能继续做干燥剂了?为了解决这个问题,老师带同学们展开探究.
[探究1]同学们用图1的装置进行实验.B烧杯中的水能被浓硫酸吸收的根本原因是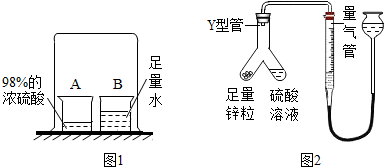
[探究2]测定探究1中吸水后硫酸溶液的溶质质量分数.
[查阅资料]H2SO4+BaCl2=BaSO4↓+2HCl;Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O
[设计实验]小组同学设计了如下三套方案,请协助他们完成实验方案的设计.
(1)取一定量的探究1所得待测溶液,滴加BaCl2 至过量,
(2)取一定量的待测溶液加入过量氧化铁,测量消耗氧化铁的质量,计算硫酸溶液的溶质质量分数.该过程发生反应的化学方程式为
(3)取一定量的待测溶液,用图2装置进行实验,利用测得的气体量,计算硫酸的质量及其浓度.该实验使Y型管中锌粒与硫酸溶液反应的正确操作是
[反思与评价]
(1)老师引导同学们对实验方案进行评价,提出问题:上述方案中,可行性差的是那一个?为什么?你的回答是
(2)聪明的小刚提出,整个探究过程通过一个实验就能实现,他的设想是
[探究1]同学们用图1的装置进行实验.B烧杯中的水能被浓硫酸吸收的根本原因是
分子在不断运动
分子在不断运动
.确认A烧杯的浓硫酸不再吸水的方法是定期多次称量硫酸的质量,而质量不变
定期多次称量硫酸的质量,而质量不变
.
[探究2]测定探究1中吸水后硫酸溶液的溶质质量分数.
[查阅资料]H2SO4+BaCl2=BaSO4↓+2HCl;Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O
[设计实验]小组同学设计了如下三套方案,请协助他们完成实验方案的设计.
(1)取一定量的探究1所得待测溶液,滴加BaCl2 至过量,
过滤、洗涤、干燥
过滤、洗涤、干燥
,称量,计算.(2)取一定量的待测溶液加入过量氧化铁,测量消耗氧化铁的质量,计算硫酸溶液的溶质质量分数.该过程发生反应的化学方程式为
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
.(3)取一定量的待测溶液,用图2装置进行实验,利用测得的气体量,计算硫酸的质量及其浓度.该实验使Y型管中锌粒与硫酸溶液反应的正确操作是
慢慢倾斜Y型管,使锌粒滑入待测溶液中
慢慢倾斜Y型管,使锌粒滑入待测溶液中
.[反思与评价]
(1)老师引导同学们对实验方案进行评价,提出问题:上述方案中,可行性差的是那一个?为什么?你的回答是
第三个,该方案中可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论
第三个,该方案中可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论
.(2)聪明的小刚提出,整个探究过程通过一个实验就能实现,他的设想是
取一定量的浓硫酸进行探究1的实验,通过测量吸水量,计算吸水后硫酸溶液的溶质质量分数
取一定量的浓硫酸进行探究1的实验,通过测量吸水量,计算吸水后硫酸溶液的溶质质量分数
.分析:[探究1]根据装置的特点及分子运动的观点解释;根据浓硫酸吸水会使质量增加分析;
[探究2][设计实验](1)根据分离难溶性物质的方法分析;
(2)硫酸和氧化铁反应产生硫酸铁和水,写出反应的方程式;
(3)倾斜使固液接触即可;
[反思与评价](1)根据各反应的测定原理对结果的影响分析;
(2)根据浓溶液稀释的原理分析.
[探究2][设计实验](1)根据分离难溶性物质的方法分析;
(2)硫酸和氧化铁反应产生硫酸铁和水,写出反应的方程式;
(3)倾斜使固液接触即可;
[反思与评价](1)根据各反应的测定原理对结果的影响分析;
(2)根据浓溶液稀释的原理分析.
解答:解:[探究1]罩在大烧杯内的浓硫酸和水没有接触,但仍能够吸水,说明分子在不停的运动着;由于浓硫酸吸水会使质量增加,因此可以通过定期多次称量硫酸的质量,而质量保持不变,说明A烧杯的浓硫酸不再吸水;
[探究2][设计实验](1)硫酸和氯化钡反应产生硫酸钡白色沉淀,可以通过硫酸钡的质量计算硫酸的质量,因此要分离硫酸钡,需要通过过滤的操作,为使结果精确,需要把硫酸钡表面附着的可溶性杂质进行洗涤、干燥;
(2)硫酸和氧化铁反应产生硫酸铁和水,反应的方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)使Y型管中锌粒与硫酸溶液反应,就要使二者接触即可,因此正确操作是:慢慢倾斜Y型管,使锌粒滑入待测溶液中;
[反思与评价](1)第(1)和第(2)个反应分别通过测定沉淀的质量、测定消耗氧化铁的质量完成计算,而第(3)个是通过测得的气体量来完成计算,但该反应可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论,所以可行性差;
(2)浓溶液吸水后会使其质量增加,增加的质量就是吸水的质量,根据浓硫酸稀释的原理即可计算吸水后硫酸溶液的溶质质量分数.
故答案为:探究1:分子在不断运动;定期多次称量硫酸的质量,而质量不变;
探究2:实验设计(1)过滤、洗涤、干燥;
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)慢慢倾斜Y型管,使锌粒滑入待测溶液中;
反思与评价:
(1)该方案中可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论;(2)取一定量的浓硫酸进行探究1的实验,通过测量吸水量,计算吸水后硫酸溶液的溶质质量分数
[探究2][设计实验](1)硫酸和氯化钡反应产生硫酸钡白色沉淀,可以通过硫酸钡的质量计算硫酸的质量,因此要分离硫酸钡,需要通过过滤的操作,为使结果精确,需要把硫酸钡表面附着的可溶性杂质进行洗涤、干燥;
(2)硫酸和氧化铁反应产生硫酸铁和水,反应的方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)使Y型管中锌粒与硫酸溶液反应,就要使二者接触即可,因此正确操作是:慢慢倾斜Y型管,使锌粒滑入待测溶液中;
[反思与评价](1)第(1)和第(2)个反应分别通过测定沉淀的质量、测定消耗氧化铁的质量完成计算,而第(3)个是通过测得的气体量来完成计算,但该反应可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论,所以可行性差;
(2)浓溶液吸水后会使其质量增加,增加的质量就是吸水的质量,根据浓硫酸稀释的原理即可计算吸水后硫酸溶液的溶质质量分数.
故答案为:探究1:分子在不断运动;定期多次称量硫酸的质量,而质量不变;
探究2:实验设计(1)过滤、洗涤、干燥;
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(3)慢慢倾斜Y型管,使锌粒滑入待测溶液中;
反思与评价:
(1)该方案中可能有氢气和二氧化硫两种气体产生,从而无法处理通过处理数据得出结论;(2)取一定量的浓硫酸进行探究1的实验,通过测量吸水量,计算吸水后硫酸溶液的溶质质量分数
点评:本题是对浓硫酸的吸水性的探究方案的评价,要充分依据题目信息结合已有的知识分析,能够考查学生的知识运用能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
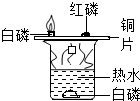 (2013?顺义区二模)如图,装置探究燃烧的条件,下列说法不正确的是( )
(2013?顺义区二模)如图,装置探究燃烧的条件,下列说法不正确的是( )