题目内容
【题目】鉴别(NH4 )2 SO4、NH4 NO3、NaNO3 三种无色溶液,随机编号为A、B、C,实验过程及现象如图所示: 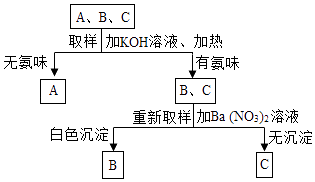
(1)A 中的溶质是;
(2)B 与 Ba(NO 3 )2 溶液混合: ①反应的化学方程式为;
②过滤,分别列出滤液中所含溶质 的所有可能情况. .
【答案】
(1)NaNO3
(2)(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3;只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物
【解析】解:铵态氮肥和碱混合加热会生成有刺激性气味的氨气,硫酸根离子和钡离子反应会生成硫酸钡沉淀,(1)A、B、C三种无色溶液加入氢氧化钠溶液、加热,A中没有氨味,B、C有氨味,所以A是硝酸钠溶液;(2)重取样品,加入硝酸钡,B中会生成白色沉淀,所以B是硫酸铵,硫酸铵和硝酸钡反应生成硫酸钡沉淀和硝酸铵,化学方程式为:(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3; 硫酸铵和硝酸钡可能恰好完全反应,可能其中的一种物质过量,所以过滤,分别列出滤液中所含溶质的所有可能情况是:只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物.
所以答案是:(1)NaNO3;(2):(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3;
只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目