题目内容
(3分)硫酸既是重要的化工产品,又是重要的化工原料,还是实验室重要的化学试剂。
(1)将浓硫酸滴到布条上,放置一会儿后可以观察到布条变成 色。
(2)浓硫酸运输过程中出现泄漏通常用熟石灰进行处理,其化学方程式为:
。
(3)浓硫酸能与金属铜反应,化学方程式为:Cu+2H2S04(浓) CuS04 +2H2O+X,X的化学式为 。
CuS04 +2H2O+X,X的化学式为 。
(1)将浓硫酸滴到布条上,放置一会儿后可以观察到布条变成 色。
(2)浓硫酸运输过程中出现泄漏通常用熟石灰进行处理,其化学方程式为:
。
(3)浓硫酸能与金属铜反应,化学方程式为:Cu+2H2S04(浓)
 CuS04 +2H2O+X,X的化学式为 。
CuS04 +2H2O+X,X的化学式为 。(3分)
(1)黑
(2)H2SO4+Ca(OH)2====CaSO4+2H2O
(3)SO2
(1)黑
(2)H2SO4+Ca(OH)2====CaSO4+2H2O
(3)SO2
分析:浓硫酸稀释时,一定要浓硫酸沿器壁慢慢注入水里,并不断用玻璃棒搅拌;切不可将水倒进浓硫酸里.可以简记为:“酸入水,沿器壁,慢慢倒,不断搅.”
解:(1)浓硫酸具有脱水性,能将布条、纸张中的氢、氧元素按水的组成比例脱去,使其碳化.
(2)硫酸与熟石灰中的氢氧化钙发生的是中和反应,注意方程式的配平.
(3)根据质量守恒定律反应前后原子种类没有改变,原子数目没有增减,通过等号两边各类原子数目相等,得出X中共有1个S原子和2个O原子,所以X的化学式为SO2.
故答案为:(1)黑;(2)H2SO4+Ca(OH)2═CaSO4+2H2O (3)SO2.
点评:书写化学方程式应注意方程式的配平,气体符号及沉淀符号的书写.
解:(1)浓硫酸具有脱水性,能将布条、纸张中的氢、氧元素按水的组成比例脱去,使其碳化.
(2)硫酸与熟石灰中的氢氧化钙发生的是中和反应,注意方程式的配平.
(3)根据质量守恒定律反应前后原子种类没有改变,原子数目没有增减,通过等号两边各类原子数目相等,得出X中共有1个S原子和2个O原子,所以X的化学式为SO2.
故答案为:(1)黑;(2)H2SO4+Ca(OH)2═CaSO4+2H2O (3)SO2.
点评:书写化学方程式应注意方程式的配平,气体符号及沉淀符号的书写.

练习册系列答案
相关题目
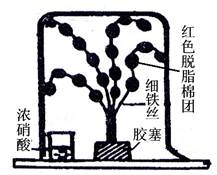
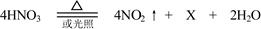 。据此回答:
。据此回答: