题目内容
(1)实验室制取二氧化碳用块状大理石或石灰石和稀盐酸;
①其反应符号表达式______.
②可用的发生装置有:______(选填上图字母序号).
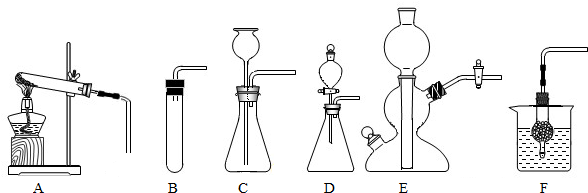
③装置E或F相对于装置C在操作方面的优势为:______.
④排水法收集与排空气法收集CO2的比较(分别用体积相同的2个集气瓶收集)
⑤写出澄清石灰水变浑浊的化学符号表达______.
(2)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
[实验一]选择合适浓度的硫酸
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表
[实验二]选择合适的反应温度
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
请根据本次活动的研究目的,分析处理以上两个表中数据,得出结论:
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为______,因为浓度小于或大于此浓度对反应的影响是______
②在合适的硫酸浓度下,应选择最合适的反应温度为______℃,因为温度高于或低于该温度对反应的影响是______
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加______操作,更有利于气体的制备.
④该研究小组为了研究______对该反应速率的影响,进行了如下实验.
①其反应符号表达式______.
②可用的发生装置有:______(选填上图字母序号).

③装置E或F相对于装置C在操作方面的优势为:______.
④排水法收集与排空气法收集CO2的比较(分别用体积相同的2个集气瓶收集)
| 比较项目 | 排水法 | 向上排空气法 |
| 收集方法可行性分析 | CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率. | CO2密度比空气大,且______ |
| 收集过程分析 | 集满现象:______ | “验满”分析因气体无色,故集满与否较难确定.即便用燃着木条移近容器口火焰熄灭,也难以证明空气完全排尽. |
| 向收集到CO2的集气瓶内倒入等体积适量澄清石灰水,并振荡 | 先浑浊后变澄清所需时间较短. | 先浑浊后变澄清所需时间较长. |
| 由上述实验可得结论 | ①______;②______. | |
(2)某研究小组在实验室制取二氧化碳的研究中发现,通常不选用大理石与稀硫酸反应制取二氧化碳,其原因是反应生成硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.为此,该小组设立研究课题:选择合适浓度的硫酸和适当的反应温度制取二氧化碳.
[实验一]选择合适浓度的硫酸
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理石的大试管中注入硫酸,记录15分钟内生成气体的体积,见下表
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积(mL) | 35 | 47 | 55 | 51 | 42 |
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度而不同温度的硫酸溶液,观察反应的情况,记录如下表:
| 试管编号 | A | B | C | D | E |
| 温度(℃) | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 |
有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应激烈,迅速产生大量气体 |
①稀硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为______,因为浓度小于或大于此浓度对反应的影响是______
②在合适的硫酸浓度下,应选择最合适的反应温度为______℃,因为温度高于或低于该温度对反应的影响是______
③除选用适当的温度和合适浓度的硫酸之外,在反应过程中,为防止硫酸钙覆盖在大理石上,应增加______操作,更有利于气体的制备.
④该研究小组为了研究______对该反应速率的影响,进行了如下实验.
| 试管编号 | A | B |
| 试管内药品 | 1g块状大理石与5mL25%稀硫酸 | 1g粉末状大理石与5mL25%稀硫酸 |
| 现象和比较 | 有少量气泡 | 迅速产生较多气泡 |
(1)①实验室制取二氧化碳用块状大理石或石灰石和稀盐酸,写出反应符号表达式的关键是,正确书写反应物CaCO3和HCl以及生成物CaCl2、H2O、CO2的化学式.
②由于实验室制取二氧化碳用块状大理石或石灰石和稀盐酸,属于固液不需要加热的反应,所以适合制取二氧化碳的发生装置有B、C、D、E、F均可;
③装置C与E、F相比最大的区别是:装置C无法控制酸的量,也就无法控制反应速度,而E、F则可以随开随用、随关随停、不与空气反应等特点.
④排水法验满的现象:集气瓶液面下降至瓶口,且瓶口有气泡冒出;
可行性分析:不与空气反应
与排空气法相比优点:排水法收集满更快,集满现象更明显;收集气体更纯净.
⑤澄清石灰水变浑浊主要是生成CaCO3沉淀.
(2)①通过表格中的数据比较不难发现当浓硫酸的浓度为25%时制的二氧化碳体积最多,高于或低于此浓度产生气体速度减慢.
②通过表格中的数据比较不难发现当反应速度为70℃时,其反应速度适中,符合要求.其它温度反应太慢或太快来不利于收集.
③不断地振荡(摇晃),可以防止硫酸钙覆盖在大理石上.
④通过表格中A和B的反应速度不难看出,固液接触面积(或固体形状)也会影响反应速度.
故答案为:
(1)①CaCO3+2HCl=CaCl2+H2O+CO2↑
②B、C、D、E、F
③随开随用随关随停;
④集气瓶液面下降至瓶口,且瓶口有气泡冒出;不与空气反应
排水法收集满更快,集满现象更明显;收集气体更纯净
⑤CO2+Ca(OH)2→CaCO3↓+H2O
(2)①25%、高于或低于此浓度产生气体速度减慢
②70、其它温度反应太慢或太快来不利于收集
③振荡(摇晃)
④固液接触面积(固体形状)
②由于实验室制取二氧化碳用块状大理石或石灰石和稀盐酸,属于固液不需要加热的反应,所以适合制取二氧化碳的发生装置有B、C、D、E、F均可;
③装置C与E、F相比最大的区别是:装置C无法控制酸的量,也就无法控制反应速度,而E、F则可以随开随用、随关随停、不与空气反应等特点.
④排水法验满的现象:集气瓶液面下降至瓶口,且瓶口有气泡冒出;
可行性分析:不与空气反应
与排空气法相比优点:排水法收集满更快,集满现象更明显;收集气体更纯净.
⑤澄清石灰水变浑浊主要是生成CaCO3沉淀.
(2)①通过表格中的数据比较不难发现当浓硫酸的浓度为25%时制的二氧化碳体积最多,高于或低于此浓度产生气体速度减慢.
②通过表格中的数据比较不难发现当反应速度为70℃时,其反应速度适中,符合要求.其它温度反应太慢或太快来不利于收集.
③不断地振荡(摇晃),可以防止硫酸钙覆盖在大理石上.
④通过表格中A和B的反应速度不难看出,固液接触面积(或固体形状)也会影响反应速度.
故答案为:
(1)①CaCO3+2HCl=CaCl2+H2O+CO2↑
②B、C、D、E、F
③随开随用随关随停;
④集气瓶液面下降至瓶口,且瓶口有气泡冒出;不与空气反应
排水法收集满更快,集满现象更明显;收集气体更纯净
⑤CO2+Ca(OH)2→CaCO3↓+H2O
(2)①25%、高于或低于此浓度产生气体速度减慢
②70、其它温度反应太慢或太快来不利于收集
③振荡(摇晃)
④固液接触面积(固体形状)

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目


